Elementárna analýza proteínov uvádza tieto priemerné hodnoty: 55% uhlíka, 7% vodíka a 16% dusíka; je zrejmé, že proteíny sa navzájom líšia, ale ich priemerné elementárne zloženie sa líši len málo od hodnôt uvedených vyššie. .
Proteíny sú ústavou makromolekuly vytvorené z prírodných α-aminokyselín; aminokyseliny sa spájajú prostredníctvom amidovej väzby, ktorá je vytvorená reakciou medzi aminoskupinou a-aminokyseliny a karboxylom inej a-aminokyseliny.
Táto väzba (-CO-NH-) sa tiež nazýva peptidová väzba, pretože viaže peptidy (kombinované aminokyseliny):
získaný je dipeptid, pretože pozostáva z dvoch aminokyselín. Pretože dipeptid obsahuje na jednom konci voľnú aminoskupinu (NH2) a karboxyl na druhom konci (COOH), môže reagovať s jednou alebo viacerými aminokyselinami a predĺžiť reťazec sprava aj zľava, a to rovnakou reakciou. vidieť vyššie.
Sled reakcií (ktoré, mimochodom, v skutočnosti nie sú také jednoduché), môže pokračovať donekonečna: kým nevznikne polymér tzv. polypeptid alebo bielkoviny. Rozdiel medzi peptidmi a proteínmi je spojený s molekulovou hmotnosťou: zvyčajne pre molekulové hmotnosti vyššie ako 10 000 hovoríme o proteínoch.
Väzba aminokyselín dohromady na získanie dokonca malých bielkovín je náročná úloha, aj keď v poslednej dobe bol vyvinutý automatický spôsob výroby bielkovín z aminokyselín, ktorý poskytuje vynikajúce výsledky.
Najjednoduchší proteín teda pozostáva z 2 aminokyselín: podľa medzinárodných zvyklostí usporiadané číslovanie aminokyselín v proteínovej štruktúre začína od aminokyseliny s voľnou a-aminoskupinou.
kódujúci tento proteín), ktorý sa stretáva s nezanedbateľnými chemickými ťažkosťami.
Usporiadanú sekvenciu aminokyselín bolo možné určiť Edmanovou degradáciou: proteín reaguje s fenylizotiokyanátom (FITC); spočiatku a-aminoskupina dusíka útočí na fenylizotiokyanát tvoriaci tiokarbamylový derivát; následne získaný produkt cyklizuje za vzniku fenyltiohydantoínového derivátu, ktorý je fluorescenčný.
Edman vyvinul stroj nazývaný sekvencer, ktorý automaticky upravuje parametre (čas, činidlá, pH atď.) Na degradáciu a poskytuje primárnu štruktúru bielkovín (za to získal Nobelovu cenu).
Primárna štruktúra nepostačuje na úplnú interpretáciu vlastností molekúl proteínu; verí sa, že tieto vlastnosti v podstatnej miere závisia od priestorovej konfigurácie, ktorú molekuly proteínu majú tendenciu predpokladať, pričom sa skladajú rôznymi spôsobmi: to znamená za predpokladu, čo bolo definované ako sekundárna štruktúra proteínov.
Sekundárna štruktúra bielkovín bliká, to znamená, že má tendenciu sa zahrievaním rozpadať; potom sa proteíny denaturujú a stratia mnohé zo svojich charakteristických vlastností. Okrem zahrievania nad 70 ° C môže byť denaturácia spôsobená aj ožiarením alebo pôsobením reaktantov (napríklad zo silných kyselín).
Denaturácia bielkovín v dôsledku tepelného účinku sa pozoruje napríklad zahrievaním vaječného bielka: stráca svoj želatínový vzhľad a mení sa na nerozpustnú bielu látku. Denaturácia proteínov však vedie k zničeniu ich sekundárnej štruktúry, ale ponechá ich primárnu štruktúru nezmenenú (zreťazenie rôznych aminokyselín).
Proteíny preberajú terciárnu štruktúru, keď sa ich reťazec, napriek tomu, že je napriek ohnutiu sekundárnej štruktúry stále flexibilný, skladá tak, že vzniká skrútené trojrozmerné usporiadanie v tvare pevného telesa. Za terciárnu štruktúru sú zodpovedné predovšetkým disulfidové väzby, ktoré je možné vytvoriť medzi cysteínom-SH rozptýleným pozdĺž molekuly.
Kvartérna štruktúra na druhej strane patrí iba k proteínom tvoreným dvoma alebo viacerými podjednotkami. Hemoglobín sa napríklad skladá z dvoch párov bielkovín (to znamená vo všetkých štyroch proteínových reťazcoch) umiestnených na vrcholoch štvorstena tak, aby vznikla sférická štruktúra; štyri proteínové reťazce sú držané pohromade iónovými silami a nekovalentné väzby.
Ďalším príkladom kvartérnej štruktúry je inzulín, ktorý sa zdá byť tvorený až šiestimi proteínovými podjednotkami usporiadanými v pároch na vrcholoch trojuholníka, v strede ktorého sú dva atómy zinku.
Vláknité proteíny
Sú to proteíny s určitou tuhosťou a majú oveľa dlhšiu os ako ostatné; vláknitý proteín prítomný vo väčších množstvách v prírode je kolagén (alebo kolagén).
Vláknitý proteín môže mať rôzne sekundárne štruktúry: a-helix, β-sheet a v prípade kolagénu triple helix; a-helix je najstabilnejšia štruktúra, po ktorej nasleduje beta-list, zatiaľ čo najmenej stabilná z týchto troch je trojzávitnica.
správny ak sa po hlavnej kostre (orientovanej zdola nahor) vykonáva pohyb podobný skrutkovaniu pravej skrutky; zatiaľ čo špirála je ľavá ruka ak je pohyb analogický so skrutkovaním ľavotočivej skrutky. V pravej a-skrutkovici sú -R substituenty aminokyselín kolmé na hlavnú os proteínu a smerujú von, zatiaľ čo vľavo- ručné a -helixy -R substituenty smerujú dovnútra. Pravostranné a-helixy sú stabilnejšie než ľavotočivé, pretože medzi vati -R c "je menšia interakcia a menej sterických prekážok. Všetky a-helixy nachádzajúce sa v proteínoch sú pravotočivé.
Štruktúra a-špirály je stabilizovaná vodíkovými väzbami (vodíkové mostíky), ktoré sú vytvorené medzi karboxylovou skupinou (-C = O) každej aminokyseliny a aminoskupinou (-NH), ktorá sa neskôr nachádza v štyroch zvyškoch lineárna postupnosť.
Príkladom proteínu so štruktúrou a-helixu je vlasový keratín.
Predĺžením štruktúry a-helixu sa uskutoční prechod z a-helixu na β-list; tiež teplo alebo mechanické napätie umožňujú prechod z a-skrutkovice do štruktúry β-listu.
V proteíne sú štruktúry ß-listu blízko seba, pretože medzi časťami samotného proteínu je možné vytvoriť medzireťazcové vodíkové väzby.
Vo vláknitých proteínoch je väčšina proteínovej štruktúry organizovaná v a-skrutkovici alebo β-vrstve.
Globulárne proteíny
Majú takmer sférickú priestorovú štruktúru (v dôsledku početných zmien v smere polypeptidového reťazca); niektoré časti bytia je možné vysledovať späť k štruktúre a-šroubovice alebo β-listu a iné časti nie sú namiesto toho prisúditeľné týmto formám: usporiadanie nie je náhodné, ale organizované a opakujúce sa.
Doteraz uvedené proteíny sú látkami úplne homogénnej konštitúcie: to znamená čistými sekvenciami kombinovaných aminokyselín; také proteíny sa hovoria jednoduché; existujú proteíny zložené z proteínovej časti a nebielkovinovej časti (skupina prostaty) nazývanej bielkoviny konjugát.
, v nechtoch, v rohovke a v očnej šošovke, medzi intersticiálnymi priestormi niektorých orgánov (napr. pečeň) a pod.
Jeho štruktúra mu dáva konkrétne mechanické schopnosti; má veľkú mechanickú pevnosť spojenú s vysokou elasticitou (napr. v šľachách) alebo vysokou tuhosťou (napr.v kostiach) v závislosti od funkcie, ktorú musí vykonávať.
Jednou z najkurióznejších vlastností kolagénu je jeho konštitučná jednoduchosť: tvorí ho asi 30% prolínu a asi 30% glycínu; ostatných 18 aminokyselín musí zdieľať iba zvyšných 40% proteínovej štruktúry. Aminokyselinová sekvencia kolagénu je pozoruhodne pravidelná: pre každé tri zvyšky je tretí glycín.
Prolín je cyklická aminokyselina, v ktorej sa skupina R viaže na a-aminodusík, čo jej dodáva určitú tuhosť.
Konečnou štruktúrou je opakujúci sa reťazec tvaru „špirály“, v kolagénovom reťazci chýbajú vodíkové väzby. Kolagén je „skrutkovica ľavej ruky s rozstupom (dĺžka zodpovedajúca jednému závitu závitnice) väčším ako„ α-skrutkovica; skrutkovica kolagénu je taká voľná, že sa tri proteínové reťazce dokážu navzájom obtočiť a vytvoriť tak „ jednoduché lano: štruktúra trojitej špirály.
Trojitá skrutkovica kolagénu je však menej stabilná ako štruktúra α-helix a β-list.
Pozrime sa teraz na mechanizmus, akým sa kolagén produkuje; zvážte napríklad prasknutie cievy: toto prasknutie je sprevádzané nespočetnými signálmi s cieľom uzavrieť cievu, čím sa vytvorí zrazenina.
Koagulácia vyžaduje najmenej tridsať špecializovaných enzýmov. Po zrazenine je potrebné pokračovať v oprave tkaniva; bunky blízko rany tiež produkujú kolagén. Za týmto účelom sa najskôr indukuje expresia génu, to znamená, že organizmy, ktoré začínajú na základe informácií o géne, sú schopné produkovať proteín (genetická informácia je transkribovaná na mRNA, ktorá opúšťa jadro a dosahuje ribozómy v cytoplazma, kde je genetická informácia preložená do proteínu). Potom sa kolagén syntetizuje v ribozómoch (vyzerá to ako skrutkovica ľavej ruky zložená z asi 1200 aminokyselín s molekulovou hmotnosťou asi 150 000 d) a potom sa hromadí v lúmenoch, kde stáva sa substrátom pre enzýmy schopné vykonávať posttranslačné modifikácie (modifikácie jazyka prekladaného „mRNA); v kolagéne tieto modifikácie spočívajú v hydroxylácii niektorých bočných reťazcov, najmä prolínu a lyzínu.
Zlyhanie enzýmov, ktoré vedú k týmto zmenám, spôsobuje skorbut: je to choroba, ktorá spočiatku spôsobuje prasknutie ciev, zlomenie zubov, po ktorom môže nasledovať interintestinálne krvácanie a smrť; môže to byť spôsobené nepretržitým používaním potravín s dlhou životnosťou.
Následne vplyvom iných enzýmov dochádza k ďalším modifikáciám, ktoré spočívajú v glykozidácii hydroxylových skupín prolínu a lyzínu (cukor sa viaže na kyslík OH); tieto enzýmy sa nachádzajú v iných oblastiach ako v lúmene, a preto proteín, ktorý prechádza úpravami, migruje do endoplazmatického retikula, aby skončil vo vreckách (vezikulách), ktoré sa samy uzatvoria a odlúčia sa od retikula: v nich je obsiahnutý glykozidovaný pro -kolagénový monomér; ten sa dostáva do Golgiho aparátu, kde konkrétne enzýmy rozpoznávajú cysteín prítomný v karboxylovej koncovej časti glykozidovaného pro-kolagénu a spôsobujú, že sa rôzne reťazce k sebe priblížia a vytvoria disulfidové mostíky: týmto spôsobom tri reťazce Glykozidovaný pro-kolagén sa získa dohromady a to je počiatočný bod, v ktorom tri reťazce, vzájomne prenikajúce, potom spontánne vedú k vzniku trojitej špirály. Tri reťazce glykoxidovaného prokolagénu spojené dohromady dosahujú potom vezikulu, ktorá, zadusí sa, oddelí sa od Golgiho aparátu a transportuje tri reťazce na perifériu bunky, kde cez fus iónu s plazmatickou membránou, je trimester vylúčený z bunky.
V mimobunkovom priestore sú konkrétne enzýmy, pro-kolagénové peptidázy, ktoré odstraňujú z druhov vylúčených z bunky, tri fragmenty (jeden pre každú skrutkovicu) 300 aminokyselín 1 ", z koncovej karboxylovej časti a tri fragmenty (jeden pre každú skrutkovicu), každý asi 100 aminokyselín, z aminoterminálnej časti: zostáva trojitá skrutkovica pozostávajúca z približne 800 aminokyselín na skrutkovicu známa ako tropokolagén.
Tropocollagen má vzhľad pomerne tuhej tyčinky; rôzne triméry sa spájajú s kovalentnými väzbami, čím vznikajú väčšie štruktúry: mikrofibrily. V mikrofibriloch sú rôzne triméry usporiadané striedavo; mnoho mikrofibríl tvorí zväzky tropokolagénu.
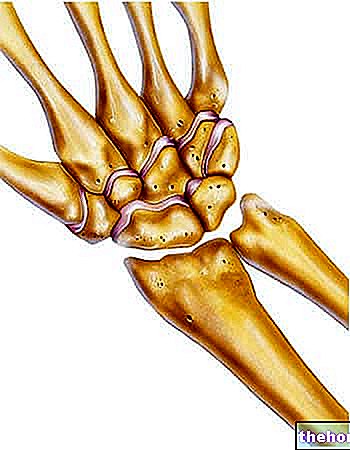
V kostiach, medzi kolagénovými vláknami, sú intersticiálne priestory, v ktorých sú uložené sírany a fosfáty vápnika a horčíka: tieto soli tiež pokrývajú všetky vlákna; to spôsobuje, že kosti sú tuhé.
V šľachách sú intersticiálne priestory menej bohaté na kryštály ako v kostiach, zatiaľ čo menšie proteíny sú prítomné v tropokolagéne: dodáva to šľachám pružnosť.
Osteoporóza je choroba spôsobená nedostatkom vápnika a horčíka, ktorá znemožňuje fixáciu solí v intersticiálnych oblastiach tropokolagénových vlákien.