Účinné látky: Brinzolamid
AZOPT 10 mg / ml očné kvapky, suspenzia
Indikácie Prečo sa používa Azopt? Načo to je?
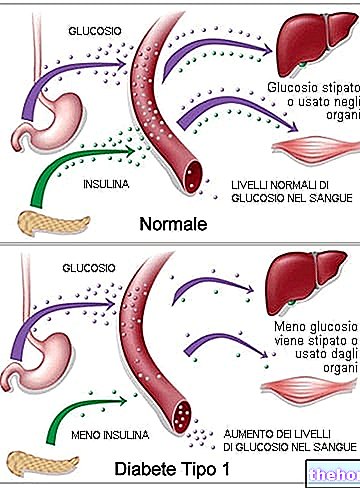
AZOPT obsahuje brinzolamid, ktorý patrí do skupiny liekov nazývaných inhibítory karboanhydrázy. Znižuje vnútroočný tlak.
Očné kvapky AZOPT sa používajú na liečbu vysokého tlaku v oku, ktorý môže viesť k glaukómu.
Ak je očný tlak príliš vysoký, môže poškodiť zrak.
Kontraindikácie Kedy by sa Azopt nemal používať
Nepoužívajte Azopt
- ak máte závažné problémy s obličkami
- ak ste alergický na niektorú zo zložiek lieku AZOPT.
- ak ste alergický na lieky nazývané sulfónamidy Medzi príklady patria lieky používané na liečbu cukrovky a infekcií, ako aj diuretiká (tablety). AZOPT môže spôsobiť rovnakú reakciu
- ak máte príliš vysokú kyslosť v krvi (stav nazývaný hyperchloremická acidóza)
Ak máte ďalšie otázky, obráťte sa na svojho lekára.
Opatrenia pri používaní Čo potrebujete vedieť predtým, ako užijete Azopt
Predtým, ako začnete používať AZOPT, obráťte sa na svojho lekára alebo lekárnika
- ak máte problémy s obličkami alebo pečeňou
- ak máte suché oči alebo problémy s rohovkou
- ak užívate iné lieky na báze sulfátu
- ak máte špecifickú formu glaukómu, pri ktorej sa vnútroočný tlak zvyšuje v dôsledku usadenín blokujúcich tok tekutiny (pseudoexfoliatívny alebo pigmentový glaukóm) alebo špecifickú formu glaukómu, pri ktorej sa vnútroočný tlak zvyšuje (niekedy rýchlo), pretože oko je tlačené dopredu a blokuje tok tekutín (glaukóm s úzkym uhlom)
Deti a dospievajúci
AZOPT by nemali používať dojčatá, deti alebo dospievajúci mladší ako 18 rokov, s výnimkou rady lekára.
Interakcie Ktoré lieky alebo potraviny môžu zmeniť účinok Azoptu
Ak užívate alebo ste v poslednom čase užívali ešte iné lieky, vrátane liekov, ktorých výdaj nie je viazaný na lekársky predpis, povedzte to svojmu lekárovi alebo lekárnikovi.
Ak užívate iný inhibítor karboanhydrázy, poraďte sa so svojim lekárom.
Upozornenia Je dôležité vedieť, že:
Tehotenstvo a dojčenie
Ak ste tehotná alebo dojčíte, ak si myslíte, že ste tehotná alebo ak plánujete otehotnieť, poraďte sa so svojím lekárom alebo lekárnikom predtým, ako začnete používať tento liek.
Ženám vo fertilnom veku sa odporúča, aby počas liečby AZOPTOM používali účinné antikoncepčné metódy. Užívanie AZOPTU sa neodporúča počas tehotenstva alebo dojčenia. Nepoužívajte AZOPT, pokiaľ to jasne neurčí váš lekár.
Pred použitím akéhokoľvek lieku sa poraďte so svojím lekárom alebo lekárnikom.
Vedenie vozidla a obsluha strojov
Neveďte vozidlo a neobsluhujte stroje, kým nie je váš zrak jasný. Bezprostredne po použití AZOPTU môže byť váš zrak nejaký čas rozmazaný.
AZOPT môže znižovať schopnosť vykonávať operácie, ktoré vyžadujú duševnú pozornosť a / alebo fyzickú koordináciu. Ak sa u vás vyskytne tento príznak, buďte opatrní pri vedení vozidla alebo obsluhe strojov.
AZOPT obsahuje benzalkóniumchlorid
AZOPT obsahuje konzervačnú látku (benzalkóniumchlorid), ktorá môže spôsobiť podráždenie očí a je známe, že odfarbuje mäkké kontaktné šošovky. Je potrebné sa vyhnúť kontaktu s mäkkými kontaktnými šošovkami. Ak nosíte kontaktné šošovky, mali by ste si ich pred nosením vybrať. Aplikácia AZOPT a počkajte najmenej 15 minút po instilácii dávky pred ich opätovným vložením.
Dávka, spôsob a čas podávania Ako používať Azopt: Dávkovanie
Vždy používajte tento liek presne tak, ako vám povedal váš lekár alebo lekárnik. Ak máte pochybnosti, poraďte sa so svojim lekárom alebo lekárnikom.
AZOPT používajte iba na oči. Neprehĺtajte a nepodávajte si injekciu.
Odporúčaná dávka je 1 kvapka do postihnutého oka, dvakrát denne - ráno a večer. Toto množstvo použite, pokiaľ vám lekár nepovie inak. AZOPT používajte do oboch očí len vtedy, ak vám to povie váš lekár. Liek používajte tak dlho, ako vám odporúča lekár.
- Získajte AZOPT a zrkadlo
- Umy si ruky
- Pretrepte fľašu a odskrutkujte uzáver. Ak sa bezpečnostný krúžok uvoľnil po odstránení uzáveru, odstráňte ho pred použitím výrobku.
- Vezmite fľašu do ruky, medzi palec a prostredník a držte ju smerom nadol
- Zakloníte hlavu dozadu. Čistým prstom stiahnite dolné viečko nadol, aby sa medzi viečkom a okom vytvorilo „vrecko“. Do oka kvapnite kvapku očných kvapiek.
- Držte hrot fľaše blízko oka. Možno vám pomôže pohľad do zrkadla
- Nedotýkajte sa oka alebo očného viečka, okolitých oblastí alebo iných povrchov špičkou fľaše, môže to infikovať očné kvapky
- Miernym tlakom na dno fľaše sa uvoľní jedna kvapka AZOPTU naraz.
- Fľašu nestláčajte: bola špeciálne navrhnutá tak, aby postačoval mierny tlak na dno
- Po použití AZOPTU zatlačte kútik oka v blízkosti nosa prstom (obrázok 3) najmenej 1 minútu. To zabraňuje šíreniu AZOPTU do zvyšku tela
- Ak potrebujete kvapky vložiť do oboch očí, zopakujte kroky pre druhé oko
- Hneď po použití nasaďte viečko späť
- Dokončite jednu fľašu pred otvorením ďalšej.
Ak kvapka chýba vášmu oku, skúste to znova.
Ak používate iné očné kvapky alebo očné masti, medzi instiláciou AZOPTU a iných očných kvapiek počkajte najmenej 5 minút. Ako posledné sa majú podávať očné masti.
Ak zabudnete použiť AZOPT
Užite jednu kvapku hneď, ako si spomeniete, a potom sa vráťte do svojich bežných časov instilácie. Nepoužívajte dvojnásobnú dávku, aby ste nahradili vynechanú dávku.
Ak prestanete užívať AZOPT
Ak prestanete používať AZOPT bez konzultácie s lekárom, váš očný tlak nebude pod kontrolou a môže viesť k strate zraku.
Predávkovanie Čo robiť, ak ste užili príliš veľa Azoptu
Ak ste nakvapkali príliš veľa očných kvapiek, okamžite si oči umyte vlažnou vodou.Kvapky nepoužívajte, kým nenastane čas na ďalšiu dávku.
Vedľajšie účinky Aké sú vedľajšie účinky lieku Azopt
Tak ako všetky lieky, aj tento liek môže spôsobovať vedľajšie účinky, hoci sa neprejavia u každého.
Pri AZOPTe boli pozorované nasledujúce vedľajšie účinky
Časté vedľajšie účinky (môžu postihnúť až 1 z 10 ľudí)
Účinky na oko: rozmazané videnie; podráždenie očí, bolesť očí, výtok z očí, svrbenie oka, suché oko, abnormálne pocity v oku, červené oči.
Všeobecné vedľajšie účinky: zlá chuť.
Menej časté vedľajšie účinky (môžu postihnúť až 1 zo 100 ľudí)
Účinky na oko: citlivosť na svetlo, zápal alebo infekcia spojovky, opuch oka, svrbivé červené alebo opuchnuté viečka, usadeniny v oku, oslnenie, pocit pálenia, rast na povrchu oka, zvýšená pigmentácia oka, únava očí, krustovanie na okraji viečka, zvýšené slzenie.
Všeobecné vedľajšie účinky: znížená funkcia srdca, rýchly alebo nepravidelný tlkot srdca, znížená srdcová frekvencia, ťažkosti s dýchaním, dýchavičnosť, kašeľ, znížený počet červených krviniek, zvýšená hladina chlóru v krvi, závraty, problémy s pamäťou, depresia, nervozita, znížené emócie, nočné mory, celková slabosť, abnormálne pocity, únava, abnormálne pocity, bolesť, problémy s pohybom, znížená sexuálna túžba, mužské sexuálne ťažkosti, symptómy chladu, prekrvenie hrudníka, infekcia nosových priechodov dutín, podráždenie hrdla, bolesť hrdlo, zvýšená alebo znížená citlivosť v ústach, zápal vnútornej strany pažeráka, bolesť brucha, nevoľnosť, vracanie, žalúdočná nevoľnosť, časté vyprázdňovanie, hnačka, črevný plyn, poruchy trávenia, bolesť obličiek, bolesť svalov, svalové kŕče, bolesť chrbta , krvácanie z nosa, nos výtok z nosa, upchatý nos, kýchanie, červená koža, abnormálne pocity na koži, hladká vyrážka alebo začervenanie so zdvihnutými hrčkami, napätie na koži, svrbenie, bolesť hlavy, sucho v ústach, úlomky v oku.
Zriedkavé vedľajšie účinky (môžu postihnúť až 1 z 1 000 ľudí)
Účinky na oko: opuch rohovky, dvojité alebo znížené videnie, abnormálne videnie, záblesky svetla v zornom poli, znížené očné pocity, opuch okolo očí, zvýšený vnútroočný tlak, poškodenie zrakového nervu.
Všeobecné vedľajšie účinky: zhoršenie pamäti, ospalosť, bolesť na hrudníku, upchatie horných dýchacích ciest, upchatie dutín, upchatý nos, sucho v nose, zvonenie v ušiach, vypadávanie vlasov, celkové svrbenie, nervozita, podráždenosť, nepravidelný srdcový tep, celková slabosť, ťažkosti spánok, dýchavičnosť, svrbivá kožná vyrážka.
Neznáme (frekvenciu nemožno odhadnúť z dostupných údajov)
Účinky na oko: abnormalita očných viečok, poruchy videnia, nepohodlie v rohovke, alergia na oči, znížený rast alebo počet rias, červené viečka.
Všeobecné vedľajšie účinky: zvýšené príznaky alergie, znížená citlivosť, chvenie, strata alebo zníženie chuti, znížený krvný tlak, zvýšený krvný tlak, zvýšený srdcový tep, bolesť kĺbov, astma, bolesť v končatinách, začervenanie, zápal alebo svrbenie kože, funkcia pečene krv abnormality testu, opuch končatín, časté močenie, znížená chuť do jedla, malátnosť.
Hlásenie vedľajších účinkov
Ak sa u vás vyskytne akýkoľvek vedľajší účinok, obráťte sa na svojho lekára alebo lekárnika. To platí aj pre akékoľvek vedľajšie účinky, ktoré nie sú uvedené v tejto písomnej informácii. Vedľajšie účinky môžete hlásiť aj priamo prostredníctvom národného systému hlásenia. Hlásením vedľajších účinkov môžete prispieť k získaniu ďalších informácií o bezpečnosti tohto lieku.
Expirácia a retencia
Tento liek uchovávajte mimo dohľadu a dosahu detí.
Nepoužívajte tento liek po dátume exspirácie, ktorý je uvedený na fľaši a škatuli po „EXP“. Dátum exspirácie sa vzťahuje na posledný deň v mesiaci.
Tento liek nevyžaduje žiadne zvláštne podmienky na uchovávanie.
Fľaša sa má zlikvidovať štyri týždne po prvom otvorení, aby sa zabránilo infekcii. Do nižšie uvedeného priestoru a do priestoru na štítok fľaše a do poľa napíšte dátum otvorenia každej fľaše. Pre balenie 1 fľaše napíšte iba 1 dátum.
Nelikvidujte lieky odpadovou vodou alebo domovým odpadom. Nepoužitý liek vráťte do lekárne. Pomáha to chrániť životné prostredie.
Ďalšie informácie
Čo AZOPT obsahuje
- Účinnou zložkou je brinzolamid. Každý mililiter obsahuje 10 mg brinzolamidu.
- Ďalšie zložky sú: benzalkóniumchlorid, karbomér 974P, dinátriumedetát, manitol (E421), čistená voda, chlorid sodný a tyloxapol. Na udržanie normálnych hodnôt kyslosti (hodnoty pH) sa pridá malé množstvo kyseliny chlorovodíkovej alebo hydroxidu sodného.
Ako vyzerá AZOPT a obsah balenia
AZOPT je mliečna očná kvapka (suspenzia) balená v 5 ml alebo 10 ml plastovej fľaši so skrutkovacím viečkom (kvapkadlo) alebo v balení obsahujúcom tri 5 ml plastové fľaše so skrutkovacím uzáverom (kvapkadlo). Nie všetky balenia musia byť na trhu.
Zdrojový leták: AIFA (Talianska agentúra pre lieky). Obsah zverejnený v januári 2016. Súčasné informácie nemusia byť aktuálne.
Aby ste mali prístup k najaktuálnejšej verzii, odporúča sa navštíviť webovú stránku AIFA (Talianska agentúra pre lieky). Vylúčenie zodpovednosti a užitočné informácie.
01.0 NÁZOV LIEKU
AZOPT 10 MG / ML OČNÉ kvapky, POZASTAVENIE
02.0 KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml suspenzie obsahuje 10 mg brinzolamidu.
Pomocné látky:
Každý ml suspenzie obsahuje 0,1 mg benzalkóniumchloridu.
Úplný zoznam pomocných látok, pozri časť 6.1.
03.0 LIEKOVÁ FORMA
Očné kvapky, suspenzia.
Biela až sivobiela suspenzia.
04.0 KLINICKÉ INFORMÁCIE
04.1 Terapeutické indikácie
AZOPT je indikovaný na zníženie vysokého vnútroočného tlaku v prípadoch:
• očná hypertenzia
• glaukóm s otvoreným uhlom
ako monoterapia u dospelých pacientov, u ktorých sa betablokátory ukázali ako neúčinné, alebo u dospelých pacientov, u ktorých sú betablokátory kontraindikované, alebo ako prídavná terapia k betablokátorom alebo analógom prostaglandínu (pozri tiež časť 5.1).
04.2 Dávkovanie a spôsob podávania
Dávkovanie
Pri použití samostatne alebo ako doplnková terapia je dávkou jedna kvapka AZOPTU do spojovkového vaku postihnutého oka (očí) dvakrát denne. Niektorí pacienti môžu mať lepšiu odpoveď jednou kvapkou trikrát denne.
Špeciálne populácie
Seniori
U starších pacientov nie je potrebná žiadna úprava dávky.
Poškodenie funkcie pečene a obličiek
AZOPT sa neskúmal u pacientov s poruchou funkcie pečene, a preto sa u týchto pacientov neodporúča.
AZOPT sa neskúmal u pacientov s ťažkým poškodením funkcie obličiek (hyperchloremická acidóza klírensu kreatinínu. Pretože brinzolamid a jeho hlavný metabolit sa vylučujú predovšetkým obličkami, AZOPT je u týchto pacientov kontraindikovaný (pozri tiež časť 4.3).
Pediatrická populácia
Bezpečnosť a účinnosť AZOPTu u dojčiat, detí a dospievajúcich vo veku 0-17 rokov neboli stanovené. V súčasnosti dostupné údaje sú popísané v častiach 4.8 a 5.1.
Použitie AZOPTu sa neodporúča u dojčiat, detí a dospievajúcich.
Spôsob podávania
Na oftalmologické použitie.
Odporúča sa nazolakrimálna oklúzia alebo pokles viečka po instilácii, čo môže znížiť systémovú absorpciu oftalmického liečiva a viesť k zníženiu systémových vedľajších účinkov.
Požiadajte pacienta, aby pred použitím fľaštičku dobre pretrepal. Po odstránení uzáveru, ak je bezpečnostný krúžok uvoľnený, ho pred použitím výrobku odstráňte.
Aby sa zabránilo kontaminácii hrotu fľaše s kvapkadlom a suspenzie, je potrebné dbať na to, aby sa hrot kvapkadla fľaše nedotýkal očných viečok, okolitých oblastí alebo iných povrchov. Informujte pacientov, aby uchovávali fľašu tesne uzavretú, ak ju nepoužívajú.
Keď sa AZOPT používa ako náhrada iného očného antiglaukómového činidla, prerušte podávanie iného lieku a na druhý deň začnite liečbu AZOPTom.
Ak sa používa viac ako jeden topický očný liek, lieky sa majú podávať jednotlivo s odstupom najmenej 5 minút. Očné masti sa majú podávať ako posledné.
Ak vynecháte dávku, pokračujte v liečbe ďalšou dávkou podľa plánu. Dávka nesmie presiahnuť jednu kvapku trikrát denne na postihnuté oko.
04.3 Kontraindikácie
• Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1.
• Známa precitlivenosť na sulfónamidy (pozri tiež časť 4.4).
• Závažná renálna insuficiencia.
• Hyperchloremická acidóza (pozri časť 4.2).
04.4 Špeciálne upozornenia a vhodné opatrenia pri používaní
Systémové efekty
AZOPT je inhibítor sulfónamid -karboanhydrázy a aj keď sa podáva lokálne, absorbuje sa systémovo. Pri topickom podávaní sa môžu vyskytnúť rovnaké typy nežiaducich reakcií, ktoré je možné prisúdiť sulfonamidom. Ak sa vyskytnú príznaky závažných reakcií. Alebo precitlivenosti, prerušte používanie tohto prípravku.
Pri perorálnom použití inhibítorov karboanhydrázy boli hlásené poruchy acidobázickej rovnováhy.Používajte opatrne u pacientov s rizikom poškodenia funkcie obličiek z dôvodu možného rizika metabolickej acidózy (pozri časť 4.2).
Účinky brinzolamidu sa neskúmali u predčasne narodených detí (gestačný vek menej ako 36 týždňov) a u detí mladších ako 1 týždeň. U pacientov s nezrelosťou alebo závažnými renálnymi tubulárnymi abnormalitami sa môže brinzolamid podávať len po starostlivom vyhodnotení rizika kvôli možnému riziku metabolickej acidózy.
Perorálne inhibítory karboanhydrázy môžu znížiť schopnosť vykonávať úlohy, ktoré si vyžadujú mentálnu pozornosť a / alebo fyzickú koordináciu. AZOPT sa absorbuje systémovo, a preto k tomu môže dôjsť pri topickom podávaní.
Súbežná terapia
Potenciál aditívneho účinku na známe systémové účinky inhibície karboanhydrázy existuje u pacientov, ktorí dostávajú perorálny inhibítor karboanhydrázy a AZOPT. Súbežné podávanie AZOPTu a perorálnych inhibítorov karboanhydrázy sa neskúmalo a neodporúča sa (pozri tiež časť 4.5 ).
AZOPT sa hodnotil hlavne pri súbežnom podávaní s timololom v doplnkovej terapii glaukómu. Skúmal sa tiež účinok AZOPT na zníženie vnútroočného tlaku (IOP) ako doplnkovej terapie k analógu prostaglandínu travoprostu. Nie sú k dispozícii žiadne dlhodobé údaje o použití AZOPTu ako prídavnej terapie k travoprostu (pozri tiež časť 5.1).
S liečbou AZOPTom sú obmedzené skúsenosti s liečbou pacientov s pseudoexfoliatívnym alebo pigmentovým glaukómom. Pri liečbe týchto pacientov je potrebná opatrnosť a je to tak
Odporúča sa prísne monitorovanie vnútroočného tlaku (IOP). AZOPT sa neskúmal u pacientov s glaukómom s úzkym uhlom a jeho použitie sa u týchto pacientov neodporúča.
Možná úloha brinzolamidu na endoteliálnych rohovkových funkciách u pacientov s narušenou rohovkou (najmä u pacientov s nízkym počtom endoteliálnych buniek) sa neskúmala.
Pacienti s kontaktnými šošovkami neboli špeciálne študovaní a u týchto pacientov sa odporúča starostlivé sledovanie počas používania brinzolamidu, pretože inhibítory karboanhydrázy môžu zmeniť hydratáciu rohovky a opotrebovanie šošoviek. Kontakt by mohol zvýšiť riziko pre rohovku. Odporúča sa dôkladné monitorovanie pacientov s poškodením rohovky, ako sú pacienti s diabetes mellitus alebo dystrofiou rohovky.
Zistilo sa, že benzalkóniumchlorid, ktorý sa bežne používa ako konzervačný prostriedok v očných výrobkoch, spôsobuje bodkovanú keratopatiu a / alebo toxickú ulceratívnu keratopatiu. Pretože AZOPT obsahuje benzalkóniumchlorid, je potrebné starostlivé sledovanie v prípade častého alebo dlhodobého používania, u pacientov so suchým okom alebo s narušením rohovky.
AZOPT sa neskúmal u nositeliek kontaktných šošoviek. AZOPT obsahuje benzalkóniumchlorid, ktorý môže spôsobiť podráždenie očí a je známe, že odfarbí mäkké kontaktné šošovky. Je potrebné sa vyhnúť kontaktu s mäkkými kontaktnými šošovkami. Pacienta treba upozorniť, aby si pred operáciou kontaktné šošovky odstránil. dávku pred ich opätovným vložením.
Možnosť rebound efektu po prerušení liečby AZOPTom sa neskúmala; účinok znižujúci vnútroočný tlak by mal trvať 5-7 dní.
Pediatrická populácia
Bezpečnosť a účinnosť AZOPTu u dojčiat, detí a dospievajúcich vo veku 0-17 rokov nebola stanovená a jeho použitie sa neodporúča u dojčiat, detí a dospievajúcich.
04.5 Interakcie s inými liekmi a iné formy interakcie
S AZOPT -om neboli vykonané žiadne špecifické štúdie liekových interakcií.V klinických štúdiách súbežné používanie AZOPT -u a očných prípravkov na báze analógov prostaglandínu a timololu neodhalilo žiadne nežiaduce interakcie. Spojenie medzi AZOPT a miotikami alebo adrenergnými agonistami nebolo hodnotené počas prídavných terapií glaukómu.
AZOPT je inhibítor karboanhydrázy a napriek tomu, že sa podáva lokálne, absorbuje sa systémovo. Pri perorálnom použití inhibítorov karboanhydrázy boli hlásené poruchy acidobázickej rovnováhy. U pacientov užívajúcich AZOPT sa má zvážiť možnosť interakcie.
Medzi izoenzýmy cytochrómu P-450 zodpovedné za metabolizmus brinzolamidu patria CYP3A4 (hlavný), CYP2A6, CYP2C8 a CYP2C9. Inhibítory CYP3A4, ako sú ketokonazol, itrakonazol, klotrimazol, ritonavir a troleandomycín, môžu inhibovať metabolizmus brinzolamidu prostredníctvom CYP3A4. Pri súbežnom použití inhibítorov CYP3A4 je potrebná opatrnosť. Pretože však eliminácia prebieha primárne obličkami, akumulácia brinzolamidu je nepravdepodobná. Brinzolamid nie je inhibítorom izoenzýmov cytochrómu P-450.
04.6 Gravidita a laktácia
Tehotenstvo
Nie sú k dispozícii alebo sú iba obmedzené údaje o oftalmickom použití brinzolamidu u gravidných žien.Štúdie na zvieratách preukázali reprodukčnú toxicitu po systémovom podaní (pozri tiež časť 5.3).
AZOPT sa neodporúča používať počas gravidity a u žien vo fertilnom veku, ktoré nepoužívajú antikoncepčné opatrenia.
Čas kŕmenia
Nie je známe, či sa brinzolamid / metabolity po topickom oftalmickom podaní vylučujú do ľudského mlieka. Štúdie na zvieratách preukázali vylučovanie minimálnych množstiev brinzolamidu do materského mlieka po perorálnom podaní.
Riziko pre novorodencov / dojčatá nemožno vylúčiť. Musí sa rozhodnúť, či prerušiť dojčenie alebo liečbu AZOPTom, pričom sa vezme do úvahy prínos dojčenia pre dieťa a prínos terapie pre ženu.
Plodnosť
Štúdie na zvieratách s brinzolamidom nepreukázali žiadny vplyv na fertilitu. Neuskutočnili sa žiadne štúdie na vyhodnotenie účinku topického oftalmického podávania brinzolamidu na fertilitu ľudí.
04.7 Účinky na schopnosť viesť vozidlá a obsluhovať stroje
AZOPT má zanedbateľný vplyv na schopnosť viesť vozidlá a obsluhovať stroje.
Dočasné rozmazané videnie alebo iné poruchy videnia môžu ovplyvniť schopnosť viesť vozidlá a obsluhovať stroje (pozri tiež časť 4.8 i). Ak sa po instilácii objaví rozmazané videnie, pacient má počkať, kým sa mu zrak nevráti. Pred vedením vozidla alebo obsluhou strojov.
Orálne inhibítory karboanhydrázy môžu narušiť schopnosť vykonávať operácie, ktoré vyžadujú duševnú pozornosť a / alebo fyzickú koordináciu (pozri tiež časť 4.4 a časť 4.8).
04.8 Nežiaduce účinky
Zhrnutie bezpečnostného profilu
V klinických skúšaniach, na ktorých sa zúčastnilo viac ako 2732 pacientov liečených AZOPTom v monoterapii alebo ako prídavok k timolol maleátu 5 mg / ml, boli najčastejšie hlásenými nežiaducimi reakciami súvisiacimi s liečbou: dysgeúzia (6,0%) (horká chuť alebo neobvyklá, pozri popis nižšie) a dočasné rozmazanie pri instilácii (5,4%) trvajúce od niekoľkých sekúnd do niekoľkých minút (pozri tiež časť 4.7).
Tabuľka nežiaducich reakcií
Nasledujúce nežiaduce reakcie boli hlásené pri očnej instilácii brinzolamidu 10 mg / ml a sú klasifikované podľa nasledujúcej konvencie: veľmi časté (≥ 1/10), časté (≥ 1/100 až
Dysgeúzia (horká alebo neobvyklá chuť v ústach po instilácii) bola najčastejšie hlásenou systémovo nežiaducou reakciou spojenou s používaním AZOPTu v klinických štúdiách; je to pravdepodobne spôsobené prechodom očných kvapiek do nosohltanu nazolakrimálnym kanálom. Nasolakrimálna oklúzia alebo mierne zatvorenie viečok po instilácii môže pomôcť znížiť výskyt tohto účinku (pozri tiež časť 4.2).
AZOPT je sulfónamidový inhibítor karboanhydrázy so systémovou absorpciou.
So systémovými inhibítormi karboanhydrázy sú vo všeobecnosti spojené gastrointestinálne, nervové, hematologické, renálne a metabolické účinky.
Pri použití AZOPTu ako prídavnej terapie k travoprostu neboli pozorované žiadne neočakávané nežiaduce reakcie. Nežiaduce reakcie pozorované pri prídavnej terapii boli pozorované pri každej jednotlivej účinnej látke.
Pediatrická populácia
V malých, krátkodobých klinických skúšaniach boli nežiaduce reakcie hlásené u približne 12,5% pediatrických pacientov, z ktorých väčšina boli lokálne, nie závažné očné reakcie, ako napríklad spojivková hyperémia, podráždenie očí, výtok z oka a zvýšené slzenie (pozri aj časť 5.1).
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité, pretože umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia. V Prílohe V.
04,9 Predávkovanie
Neboli hlásené žiadne prípady predávkovania. Liečba má byť symptomatická a podporná. Môže sa vyskytnúť nerovnováha elektrolytov, vývoj stavu acidózy a možné účinky na nervový systém. Je potrebné monitorovať hladiny elektrolytu v sére (najmä draslíka) a hladiny pH v krvi.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antiglaukómy a miotické prípravky, inhibítory karboanhydrázy.
ATC kód: S01EC04.
Mechanizmus akcie
Karboanhydráza je enzým nachádzajúci sa v mnohých tkanivách tela vrátane oka. Karboanhydráza katalyzuje reverzibilnú reakciu, ktorá zahŕňa hydratáciu oxidu uhličitého a dehydratáciu kyseliny uhličitej.
Inhibícia karboanhydrázy na úrovni mihalnicových procesov oka znižuje sekréciu komorovej vody, pravdepodobne v dôsledku spomalenia tvorby hydrogénuhličitanových iónov s následným znížením transportu sodíka a tekutiny. Výsledkom je zníženie vnútroočného tlaku (VOT), hlavného rizikového faktora v patogenéze poškodenia zrakového nervu a straty zorného poľa pri glaukóme. Brinzolamid, inhibítor karboanhydrázy II (CA-II), prevládajúceho izoenzýmu v oku, s IC50 in vitro 3,2 nM a Ki 0,13 nM voči CA-II.
Klinická účinnosť a bezpečnosť
Bol skúmaný účinok AZOPT na zníženie vnútroočného tlaku (IOP) ako doplnkovej terapie k analógu prostaglandínu travoprostu. Po úvodnej 4-týždňovej liečbe travoprostom boli pacienti s IOP ≥19 mmHg randomizovaní na ďalšiu liečbu brinzolamidom alebo timololom. Došlo k "ďalšiemu zníženiu priemerného denného vnútroočného tlaku z 3,2 na 3,4 mmHg v skupine s brinzolamidom a z 3,2 na 4,2 mmHg v skupine s timololom. Došlo k" výskytu Celkove vyšší v nezávažných očných nežiaducich reakciách, ktoré sa týkali predovšetkým znakov lokálne podráždenie, v skupinách s brinzolamidom / travoprostom. Udalosti boli mierne a neovplyvnili celkovú mieru prerušenia štúdie (pozri tiež časť 4.8).
Klinická štúdia s AZOPT bola vykonaná u 32 pediatrických pacientov mladších ako 6 rokov, u ktorých bol diagnostikovaný glaukóm alebo očná hypertenzia. Niektorí pacienti nikdy nepodstúpili očnú hypotonizačnú liečbu, zatiaľ čo iní už boli liečení inými. Lieky znižujúce vnútroočný tlak. nemusí ukončiť liečbu, kým sa nezačne monoterapia AZOPTom.
U pacientov, ktorí nikdy nepodstúpili očnú hypotonickú terapiu (10 pacientov), bola účinnosť AZOPT podobná tej, ktorá bola predtým pozorovaná u dospelých jedincov, so znížením priemerného vnútroočného tlaku až o 5 mmHg od východiskového stavu. Pacienti, ktorí boli na topickej terapii znižujúcej vnútroočný tlak (22 pacientov), priemerný VOT sa mierne zvýšil od východiskového stavu v skupine s AZOPT.
05.2 Farmakokinetické vlastnosti
Po topickom očnom podaní sa brinzolamid absorbuje do systémového obehu. Vzhľadom na vysokú afinitu k karboanhydráze II je brinzolamid vo veľkej miere distribuovaný v červených krvinkách a má dlhý polčas v plnej krvi (to znamená približne 24 týždňov). U ľudí sa tvorí metabolit N-desetyl brinzolamid. Ktorý sa tiež viaže na karboanhydrázu a hromadí sa v červených krvinkách. Tento metabolit sa v prítomnosti brinzolamidu viaže predovšetkým na karboanhydrázu I. V plazme sú koncentrácie brinzolamidu aj N-desetyl brinzolamidu nízke a vo všeobecnosti sú pod hranicou kvantitatívnej analýzy (
Väzba na plazmatické bielkoviny nie je vysoká (približne 60%).Eliminácia metabolity N-desmetoxypropyl a O-desmetyl.
V orálnej farmakokinetickej štúdii dostávali zdraví dobrovoľníci 1 mg kapsuly brinzolamidu dvakrát denne počas 32 týždňov a na stanovenie stupňa systémovej inhibície karboanhydrázy sa merala aktivita karboanhydrázy v červených krvinkách.
Nasýtenie červených krviniek karboanhydrázou II brinzolamidom sa dosiahlo do štyroch týždňov (koncentrácie červených krviniek približne 20 μM). N-desetyl brinzolamid nahromadený v červených krvinkách dosiahol ustálený stav v priebehu 20-28 týždňov s koncentráciami medzi 6 a 30 mcM. Inhibícia celkovej aktivity karboanhydrázy v červených krvinkách v rovnovážnom stave bola približne 70-75%.
Jedinci so stredne ťažkou poruchou funkcie obličiek (klírens kreatinínu 30-60 ml / min) dostávali 1 mg brinzolamidu perorálne dvakrát denne až 54 týždňov. Koncentrácia liečiva v červených krvinkách vo štvrtom týždni liečby sa pohybovala od približne 20 do 40 mcM. V rovnovážnom stave sa koncentrácie brinzolamidu a jeho metabolitu v červených krvinkách pohybovali od 22,0 do 46,1, respektíve 17,1 až 88,6 mcM.
Koncentrácia N-desetyl-brinzolamidu v červených krvinkách sa zvýši a aktivita celkovej karboanhydrázy v červených krvinkách sa zníži znížením eliminácie kreatínu, ale koncentrácia brinzolamidu v červených krvinkách a aktivita CA-II zostáva nezmenená. U subjektov s najvyššou úrovňou renálnej dysfunkcie bola inhibícia celkovej aktivity karboanhydrázy vyššia, aj keď v rovnovážnom stave menej ako 90%.
V topickej očnej štúdii boli koncentrácie brinzolamidu v červených krvinkách v rovnovážnom stave podobné tým, ktoré sa zistili v orálnej štúdii, ale hladiny N-desetyl brinzolamidu boli nižšie. Aktivita karboanhydrázy bola približne 40-70% hladín pred dávkou
05.3 Predklinické údaje o bezpečnosti
Predklinické údaje na základe obvyklých štúdií farmakologickej bezpečnosti, toxicity po opakovanom podávaní, genotoxicity a karcinogénneho potenciálu neodhalili žiadne osobitné riziko pre ľudí.
Štúdie vývojovej toxicity na králikoch s perorálnymi dávkami brinzolamidu do 6 mg / kg / deň (125 -násobok odporúčanej očnej dávky pre ľudí) neodhalili žiadne účinky na vývoj plodu napriek významnej toxicite pre matku. Podobné štúdie na potkanoch ukázali mierne zníženú osifikáciu lebky a hrudnej kosti plodov matiek, ktorým bol podávaný brinzolamid v dávke 18 mg / kg / deň (375 -násobok odporúčanej očnej dávky pre ľudí), ale nie v dávkach 6 mg / kg / deň. Tieto výsledky sa vyskytli pri dávkach, ktoré spôsobovali metabolickú acidózu so znížením rastu telesnej hmotnosti matky a hmotnosti plodu. Na potomstve matiek, ktoré dostávali brinzolamid perorálne s rôznym poklesom (približne 5-6%) pri 2 mg / kg / deň na približne 14% pri 18 mg / deň. Kg / deň, bolo pozorované na dávke závislé zníženie hmotnosti plodu. Počas laktácie bola hladina bez vedľajších účinkov u potomstva 5 mg / kg / deň.
06.0 FARMACEUTICKÉ INFORMÁCIE
06.1 Pomocné látky
Benzalkóniumchlorid,
manitol (e421),
karbomér 974p,
tyloxapol,
edetát dvojsodný,
chlorid sodný,
kyselina chlorovodíková / hydroxid sodný (na úpravu pH)
vyčistená voda.
06.2 Nekompatibilita
Nie je to relevantné.
06.3 Obdobie platnosti
2 roky.
4 týždne po prvom otvorení.
06.4 Špeciálne opatrenia na uchovávanie
Tento liek nevyžaduje žiadne zvláštne podmienky na uchovávanie.
06.5 Charakter vnútorného obalu a obsahu balenia
Nepriehľadné polyetylénové fľaše s nízkou hustotou s polypropylénovým skrutkovacím uzáverom 5 ml a 10 ml.
K dispozícii sú nasledujúce veľkosti balenia: balenie obsahujúce 1 x 5 ml, 3 x 5 ml a 1 x 10 ml.
Nie všetky balenia musia byť na trhu.
06.6 Návod na použitie a zaobchádzanie
Žiadne špeciálne pokyny.
07.0 DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Alcon Laboratories (UK) Ltd.
Business park Frimley
Frimley
Camberley
Surrey GU16 7SR
UK.
08.0 REGISTRAČNÉ ČÍSLO
5 ml fľaša: EU/1/00/129/001 (AIC č.034770014/E)
10 ml fľaša: EU/1/00/129/002 (AIC č.034770026/E)
3 fľaše po 5 ml: EU/1/00/129/003
09.0 DÁTUM PRVEJ REGISTRÁCIE ALEBO OBNOVENIA REGISTRÁCIE
Dátum prvej registrácie: 9. marca 2000
Dátum posledného obnovenia: 9. marca 2005
10.0 DÁTUM REVÍZIE TEXTU
D.CCE, apríl 2015