Definícia osmózy
Osmóza je spontánny prechod rozpúšťadla (ktorým je v biologických systémoch obvykle voda) z roztoku, v ktorom sú rozpustené látky viac riedené, na roztok, v ktorom sú koncentrovanejšie; tento pohyb - ktorý prebieha prostredníctvom polopriepustnej membrány - pokračuje, až kým sa nedosiahne rovnovážna situácia, v ktorej oba roztoky získavajú a udržiavajú rovnakú koncentráciu.
Praktický príklad

Aby sme lepšie objasnili koncept osmózy, predstavme si, že máme nádobu rozdelenú na dve oddelenia rovnakého objemu (A a B) semipermeabilnou membránou (to znamená, že je priepustná iba pre rozpúšťadlo - v tomto prípade pre vodu - a nie pre rozpustená látka). oddelenie A je vodný roztok, v ktorom bola rozpustená polievková lyžica glukózy, zatiaľ čo v časti B máme vodný roztok rovnakého objemu, v ktorom sú rozpustené tri polievkové lyžice glukózy (je teda koncentrovanejší). rozdiel vytvára gradient koncentrácie glukózy na stranách membrány, a pretože tento cukor ju nemôže prekročiť, rovnováha sa dosiahne prechodom vody z oddelenia A (kde je glukóza zriedenejšia) do oddelenia B (kde je hojnejšie) ). Ak chcete, dá sa tiež povedať, že voda prechádza osmózou z roztoku, v ktorom je koncentrovanejšia (A), do toho, v ktorom je menej koncentrovaná (B).
Po tomto prietoku sa hladina vody v B zvyšuje a klesá v A, čím medzi nimi vzniká určitý hladinový rozdiel. Tento jav sa končí, keď tieto dva roztoky dosiahnu rovnakú koncentráciu a potom ju udržujú konštantnú.
Hypotonické, izotonické a hypertonické riešenia
Keď sa vezmú dva roztoky s rôznou molárnou koncentráciou (rôzny počet častíc v nich rozpustených), roztok s najnižšou molárnou koncentráciou je definovaný ako hypotonický a koncentrovanejší je hypertonický. Dva roztoky sú namiesto toho izotonické (alebo ekvimolárne), ak majú rovnakú koncentráciu.
V práve uvedenom príklade je roztok B hypertonický (preto obsahuje viac rozpustených látok) ako ten druhý (definovaný ako hypotonický); preto sa za normálnych podmienok rozpúšťadlo pohybuje osmózou z hypotonického do hypertonického roztoku. Hovorili sme o štandardných podmienkach, pretože hraním sa s fyzikálnymi zákonmi je možné prevrátiť samotný koncept osmózy a uprednostniť prechod rozpúšťadla z najriedenejšej koncentrácie do najkoncentrovanejšej (reverzná osmóza).
Osmotický tlak a reverzná osmóza
Ako je zatiaľ vyjadrené, čistý tok rozpúšťadla - generovaný osmózou - pokračuje, kým tieto dva roztoky nedosiahnu rovnakú koncentráciu. Tento pohyb je možné potlačiť, zastaviť alebo dokonca zvrátiť tlakom na oddelenie s najvyššou koncentráciou.

V predchádzajúcom príklade stačí umiestniť piest do oddelenia B (u ktorého si pamätáme, že má vyššiu koncentráciu) a stlačiť ho určitou silou, aby sa podporil prechod vody smerom k A; v tomto prípade hovoríme o obrátení osmóza.
Osmotický tlak je tlak, ktorý je presne proti prechodu rozpúšťadla cez semipermeabilnú membránu; v dôsledku toho je to tlak potrebný na pôsobenie proti osmóze.
Pokiaľ ide o to, čo bolo doteraz povedané, dve izotonické roztoky majú rovnaký osmotický tlak; treba preto zdôrazniť, že osmotický tlak závisí výlučne od počtu častíc prítomných v roztoku, a nie od ich povahy.
Osmóza a ľudské telo
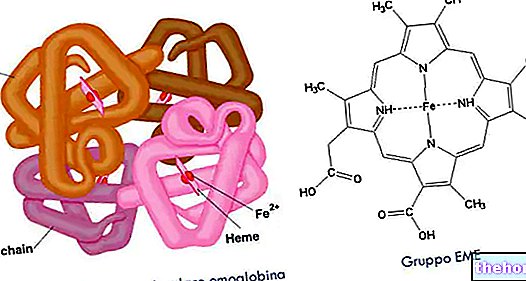
Plazmatické membrány, ktoré obklopujú bunky ľudského tela, sú v skutočnosti polopriepustné membrány, ktoré umožňujú priamym prechodom malých molekúl (ako je voda a močovina) prostredníctvom osmózy, ale nie tých, ktoré majú väčšiu molekulovú hmotnosť ( proteíny, aminokyseliny a cukry). Osmotické rovnováhy v telesných tekutinách sú preto nevyhnutné na zabezpečenie optimálneho prostredia pre bunky.
Ak vezmeme bunku ako červenú krvinku a ponoríme ju do hypotonického roztoku, tento - osmózou - dôjde k opuchu (spôsobenému vstupom vody), ktorý môže dokonca spôsobiť jej výbuch. Naopak, ak je ponorený do hypertonický roztok bunka, ktorú podstúpi, v dôsledku prechodu vody von, závažnej dehydratácii, ktorá spôsobuje jej vrásky. Našťastie sú bunky ľudského tela ponorené do izotonických roztokov s ohľadom na ich vnútorné prostredie a existujú rôzne systémy na udržanie týchto kvapalín v osmotickej rovnováhe.
Osmotický tlak a skladovanie potravín
Zamyslime sa chvíľu nad domácim džemom ... cukor sa pridáva v hojnom množstve nielen na zlepšenie chuti, ale aj a predovšetkým na zvýšenie trvanlivosti. Cukor je však dôležitým prvkom pre život mnohých mikroorganizmov, ktoré sa podieľajú na degradácii produktu. Tento zdanlivý rozpor je odstránený samotným konceptom osmózy.