Účinné látky: folitropín beta
Puregon 50 IU / 0,5 ml injekčný roztok
Puregon 75 IU / 0,5 ml injekčný roztok
Puregon 100 IU / 0,5 ml injekčný roztok
Puregon 150 IU / 0,5 ml injekčný roztok
Puregon 200 IU / 0,5 ml injekčný roztok
Puregon 225 IU / 0,5 ml injekčný roztok
Príbalové letáky Puregon sú k dispozícii pre veľkosti balenia: - Puregon 50 IU / 0,5 ml injekčný roztok, Puregon 75 IU / 0,5 ml injekčný roztok, Puregon 100 IU / 0,5 ml injekčný roztok, Puregon 150 IU / 0,5 ml injekčný roztok, Puregon 200 IU / 0, 5 ml roztok na injekcia, Puregon 225 IU / 0,5 ml injekčný roztok
- Puregon 150 IU / 0,18 ml injekčný roztok, Puregon 300 IU / 0,36 ml injekčný roztok, Puregon 600 IU / 0,72 ml injekčný roztok, Puregon 900 IU / 1,08 ml injekčný roztok
Prečo sa používa Puregon? Načo to je?
Injekčný roztok Puregon obsahuje folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH).
FSH patrí do skupiny gonadotropínov, ktoré hrajú dôležitú úlohu v plodnosti a reprodukcii človeka.U žien je FSH nevyhnutný pre rast a dozrievanie folikulov vo vaječníkoch. Folikuly sú malé, okrúhle vezikuly, ktoré obsahujú vaječné bunky. U ľudí je FSH potrebný na produkciu spermií.
Puregon sa používa na liečbu neplodnosti v ktoromkoľvek z nasledujúcich stavov:
ženy
U žien, ktoré nemajú ovuláciu a ktoré nereagujú na liečbu citrátom klomifénu, možno na vyvolanie ovulácie použiť Puregon. U žien podstupujúcich techniky asistovanej reprodukcie vrátane oplodnenia in vitro (IVF) a iných metód môže Puregon indukovať rozvoj folikuly.
Muži
U mužov, ktorí majú neplodnosť v dôsledku nízkych hladín hormónov, možno Puregon použiť na produkciu spermií.
Kontraindikácie Kedy by sa Puregon nemal používať
Nepoužívajte Puregon, ak:
- ste alergický na folitropín beta alebo na ktorúkoľvek z ďalších zložiek Puregonu (uvedených v časti 6)
- máte rakovinu vaječníkov, prsníka, maternice, semenníkov alebo mozgu (hypofýza alebo hypotalamus)
- máte závažné alebo nepravidelné vaginálne krvácanie neznámeho pôvodu
- máte nefungujúce vaječníky, pretože máte stav nazývaný primárne zlyhanie vaječníkov
- máte ovariálne cysty alebo zväčšené vaječníky, ktoré nie sú spôsobené syndrómom polycystických vaječníkov (PCOS)
- má malformácie pohlavných orgánov, ktoré znemožňujú normálne tehotenstvo
- má maternicové myómy, ktoré znemožňujú normálne tehotenstvo
- ste muž a ste neplodný pre stav nazývaný primárne zlyhanie semenníkov.
Opatrenia pri používaní Čo potrebujete vedieť predtým, ako užijete Puregon
Pred použitím Puregonu sa poraďte so svojim lekárom, ak:
- ste mali alergickú reakciu na niektoré antibiotiká (neomycín a / alebo streptomycín)
- máte nekontrolovanú hypofýzu alebo problémy s hypotalamom
- majú zníženú činnosť štítnej žľazy (hypotyreóza)
- máte nadobličky, ktoré nefungujú správne (adrenokortikálna insuficiencia)
- máte vysoké hladiny prolaktínu v krvi (hyperprolaktinémia)
- máte akékoľvek iné zdravotné ťažkosti (napríklad cukrovku, srdcové choroby alebo akékoľvek iné dlhodobé ochorenie).
Ak ste žena:
Ovariálny hyperstimulačný syndróm (OHSS)
Váš lekár bude pravidelne kontrolovať účinky liečby, aby bol schopný zvoliť si primeranú dávku Puregonu každý deň. V pravidelných intervaloch môže vykonávať ultrazvukové vyšetrenie vaječníkov. Lekár môže tiež skontrolovať hladiny hormónov v krvi. Je to veľmi dôležité, pretože príliš vysoká dávka FSH môže spôsobiť zriedkavé, ale závažné komplikácie, pri ktorých dochádza k nadmernej stimulácii vaječníkov a rastu folikulov nad normál. Tento závažný zdravotný stav sa nazýva ovariálny hyperstimulačný syndróm (OHSS). V zriedkavých prípadoch môže závažný OHSS ohrozovať život. OHSS spôsobuje náhle nahromadenie tekutiny v oblastiach žalúdka a hrudníka a môže spôsobiť tvorbu krvných zrazenín. Okamžite zavolajte lekára, ak spozorujete silný opuch brucha, bolesť v oblasti žalúdka (brucha), pocit nevoľnosti (nauzea), vracanie, náhle zvýšenie telesnej hmotnosti v dôsledku hromadenia tekutín, hnačku, znížené vylučovanie moču alebo problémy s dýchaním (pozri tiež časť 4 o možných vedľajších účinkoch).
Pravidelné sledovanie reakcie na liečbu FSH pomáha predchádzať ovariálnej hyperstimulácii. Ak pocítite bolesť žalúdka, aj keď k tomu dôjde niekoľko dní po poslednej injekcii, ihneď kontaktujte svojho lekára.
Viacnásobné tehotenstvo alebo vrodené chyby
Po liečbe gonadotropínovými prípravkami existuje zvýšená pravdepodobnosť viacpočetného tehotenstva, aj keď sa do maternice prenesie iba jedno embryo. Viacnásobné tehotenstvo vedie k zvýšenému zdravotnému riziku pre matku i dieťa v prvom období života. Okrem toho môže byť viacpočetné tehotenstvo a charakteristiky pacientok podstupujúcich liečbu plodnosti (napr. Vek ženy, vlastnosti spermií, genetické pozadie oboch rodičov) spojené so zvýšeným rizikom vrodených chýb.
Komplikácie tehotenstva
Mierne sa zvyšuje riziko tehotenstva mimo maternice (mimomaternicové tehotenstvo), Lekár by preto mal vykonať včasné ultrazvukové vyšetrenie, aby vylúčil možnosť tehotenstva mimo maternice.
U žien podstupujúcich liečbu neplodnosti môže byť možnosť potratu o niečo vyššia.
Krvná zrazenina (trombóza)
Liečba Puregonom, podobne ako samotné tehotenstvo, môže zvýšiť riziko vzniku krvnej zrazeniny (trombózy). Trombóza je tvorba krvnej zrazeniny v cieve.
Krvné zrazeniny môžu mať za následok vážne zdravotné stavy, ako napríklad:
- upchatie pľúc (pľúcna embólia)
- mŕtvica
- infarkt
- problémy s krvnými cievami (tromboflebitída)
- nedostatočný prietok krvi (hlboká žilová trombóza), ktorý môže spôsobiť stratu ruky alebo nohy.
Pred začatím liečby sa poraďte so svojim lekárom, najmä:
- ak už viete, že máte zvýšenú pravdepodobnosť vzniku trombózy
- ak ste sami mali trombózu alebo ju mal niekto z vašej najbližšej rodiny
- ak máte veľkú nadváhu.
Torzia vaječníkov
Po liečbe gonadotropínmi vrátane Puregonu došlo k torzii vaječníkov. Torzia vaječníkov je skrútenie vaječníka. Skrútenie vaječníka by mohlo spôsobiť „prerušenie“ prívodu krvi do vaječníka.
Skôr ako začnete používať tento liek, povedzte to svojmu lekárovi, ak:
- ste niekedy mali syndróm ovariálnej hyperstimulácie OHSS
- ste tehotná alebo máte podozrenie na tehotenstvo
- ste niekedy mali operáciu žalúdka (brucha)
- ste niekedy mali skrútenie vaječníka
- ste niekedy mali alebo v súčasnosti máte cysty v jednom alebo oboch vaječníkoch.
Ovariálne a iné rakoviny reprodukčného systému
U žien, ktoré podstúpili liečbu neplodnosti, sa vyskytli prípady rakoviny vaječníkov a iných rakovín reprodukčného systému. Nie je známe, či liečba liekmi na plodnosť zvyšuje riziko týchto rakovín u neplodných žien.
Iné zdravotné stavy
Tiež skôr, ako začnete používať tento liek, povedzte to svojmu lekárovi, ak:
- Váš lekár vám povedal, že tehotenstvo môže byť pre vás nebezpečné.
Ak ste muž:
Muži s príliš veľkým množstvom FSH v krvi
Zvýšené hladiny FSH v plazme sú znakom poškodenia semenníkov. Puregon v týchto situáciách zvyčajne nie je účinný. Na kontrolu účinkov liečby môže váš lekár požiadať o analýzu vzorky spermy, štyri až šesť mesiacov po operácii. “Začiatok terapie.
Interakcie Aké lieky alebo potraviny môžu zmeniť účinok Puregonu
Ak teraz užívate alebo ste v poslednom čase užívali, či práve budete užívať ďalšie lieky, povedzte to svojmu lekárovi alebo lekárnikovi.
Súbežné používanie Puregonu a klomiféncitrátu môže zvýšiť účinok Puregonu. Ak dostávate agonistu GnRH (liek používaný na zabránenie predčasnej ovulácii), možno budete potrebovať vyššiu dávku Puregonu.
Upozornenia Je dôležité vedieť, že:
Tehotenstvo a dojčenie
Skôr ako začnete užívať akýkoľvek liek, poraďte sa so svojím lekárom alebo lekárnikom. Puregon by ste nemali používať, ak ste tehotná alebo máte podozrenie, že ste tehotná.
Puregon môže ovplyvniť produkciu mlieka. Je nepravdepodobné, že by Puregon prechádzal do materského mlieka. Ak dojčíte, povedzte to svojmu lekárovi pred použitím Puregonu.
Vedenie vozidla a obsluha strojov
Je nepravdepodobné, že by Puregon ovplyvnil vašu schopnosť viesť vozidlo alebo obsluhovať stroje.
Dôležité informácie o niektorých zložkách Puregonu
Tento liek obsahuje menej ako 1 mmol (23 mg) sodíka v jednej injekcii, tj. Je v zásade „bez sodíka“.
Deti
Použitie Puregonu u detí nie je relevantné.
Dávkovanie a spôsob použitia Ako používať Puregon: Dávkovanie
Vždy používajte tento liek presne tak, ako vám povedal váš lekár. Ak máte pochybnosti, poraďte sa so svojim lekárom alebo lekárnikom.
Dávkovanie u žien
Váš lekár rozhodne o začiatočnej dávke. Túto dávku je možné počas liečebného obdobia upraviť. Ďalšie podrobnosti o pláne liečby sú uvedené nižšie.
V odpovedi vaječníkov na FSH sú medzi ženami a ženami významné rozdiely; preto nie je možné definovať dávkovací režim, ktorý by vyhovoval všetkým pacientkam. Na určenie vhodného dávkovania bude lekár sledovať rast folikulu ultrazvukovým vyšetrením a meranie množstva estradiolu (ženského pohlavného hormónu) v krvi.
- Ženy, ktoré nemajú ovuláciu
Lekár stanoví počiatočnú dávku. Táto dávka sa udržiava najmenej 7 dní. Ak nedôjde k ovariálnej odpovedi, denná dávka sa postupne zvyšuje, kým veľkosť folikulu a / alebo plazmatické hladiny estradiolu nevykazujú vhodnú odpoveď. Denná dávka sa potom udržiava, kým sa nezistí prítomnosť vhodne veľkého folikulu. 7-14 dní liečby je spravidla dostačujúce. Liečba Puregonom sa potom zastaví a ovulácia sa vyvolá podaním ľudského chorionického gonadotropínu (hCG).
- Programy asistovanej reprodukcie, ako napríklad IVF
Lekár stanoví počiatočnú dávku. Táto dávka sa udržiava najmenej prvé štyri dni. Dávku je potom možné upraviť podľa reakcie vaječníkov. Keď je prítomný príslušný počet folikulov adekvátnej veľkosti, konečná fáza dozrievania sa vyvolá podaním hCG. Odber vajíčka (vajíčok) sa vykoná o 34-35 hodín neskôr.
Dávkovanie u človeka
Puregon sa zvyčajne predpisuje v dávke 450 IU týždenne, väčšinou rozdelených do 3 dávok po 150 IU, v kombinácii s podávaním iného hormónu (hCG), najmenej na 3-4 mesiace. Obdobie liečby sa rovná času vývoja spermií a času, kedy sa očakáva zlepšenie. Ak sa produkcia spermií nezačne po tomto čase, terapia môže pokračovať najmenej 18 mesiacov.
Ako sa má injekcia podať
Prvá injekcia Puregonu sa má podať iba v prítomnosti lekára alebo zdravotnej sestry. Injekcia sa podáva pomaly do svalu (napríklad do zadku, stehna alebo nadlaktia) alebo pod kožu (napríklad do spodnej časti žalúdka).
Ak sa podáva do svalu, injekciu má podať lekár alebo zdravotná sestra.
Ak sa podá pod kožu, injekciu môže v niektorých prípadoch podať sám alebo iná osoba. Váš lekár vám povie, kedy a ako podať injekciu. Ak si podávate Puregon sami, riaďte sa pokynmi na použitie v nasledujúcej časti, aby sa Puregon podával správne a s minimálnym nepríjemným pocitom.
Inštrukcie na používanie
Krok 1 - Príprava injekčnej striekačky
Na podanie Puregonu sa majú použiť sterilné jednorazové injekčné striekačky a ihly. Objem injekčnej striekačky by mal byť dostatočne malý, aby bolo možné predpísanú dávku podať s primeranou presnosťou.
Injekčný roztok Puregon sa dodáva v sklenenej injekčnej liekovke. Ak roztok obsahuje častice alebo nie je číry, nemá sa použiť. Najprv musíte z injekčnej liekovky odstrániť vyklápací uzáver. Vložte ihlu do injekčnej striekačky a prepichnite gumovú zátku injekčnej liekovky ihlou. Natiahnite roztok do injekčnej striekačky a použitú ihlu nahraďte injekčnou ihlou.
Nakoniec držte injekčnú striekačku tak, aby ihla smerovala nahor, a jemne poklepte na samotnú striekačku, aby ste prinútili vzduchové bubliny stúpať nahor; potom zatlačte piest, kým sa vzduch nevytlačí a v injekčnej striekačke zostane iba roztok Puregon .. V prípade potreby je možné piest znova zatlačiť, kým sa neupraví podávaný objem.
Krok 2 - Miesto vpichu
Najlepším miestom na podanie pod kožu je spodná časť žalúdka okolo pupka (ov), kde je značné množstvo voľnej kože a vrstvy tuku. Pri každom ošetrení sa bude musieť miesto vpichu mierne líšiť.
Je možné podať injekciu aj do iných oblastí. Váš lekár alebo zdravotná sestra vám povie, kam si máte podať injekciu.
Krok 3 - Príprava miesta vpichu
Niekoľko klepnutí na miesto vpichu stimuluje jemné nervové zakončenia a pomôže zmierniť nepohodlie spôsobené vpichom ihly. Umyte si ruky a miesto vpichu dezinfikujte dezinfekčným prostriedkom (napr. 0,5%chlórhexidín), aby ste odstránili baktérie z povrchu. Vyčistite asi 5 cm okolo bodu, kde ihla prenikne, a nechajte oblasť najmenej jednu minútu vyschnúť, než budete pokračovať.
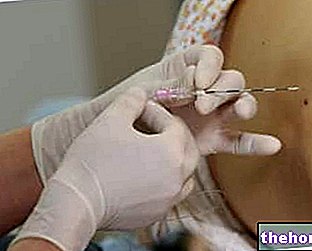
Krok 4 - Zavedenie ihly
Stisnite oblasť pokožky medzi dvoma prstami. Druhou rukou vpichnite ihlu so sklonom 90 ° vzhľadom na samotný povrch kože, ako je znázornené na obrázku.
Krok 5 - Kontrola správnej polohy ihly
Ak je poloha ihly správna, malo by byť obtiažne zasunúť piest. Akákoľvek krv v injekčnej striekačke naznačuje, že sa ihla dostala do žily alebo tepny. Ak sa to stane, vyberte ihlu, miesto vpichu prikryte tampónom navlhčeným dezinfekčným prostriedkom a zatlačte naň; krv sa zastaví za 1 až 2 minúty. Nepoužívajte roztok obsiahnutý v injekčnej striekačke. Potom začnite od kroku 1 znova pomocou novej injekčnej striekačky, nových ihiel a novej injekčnej liekovky Puregonu.
Krok 6 - Vstreknite roztok
Zatláčajte piest pomaly a stabilne, aby bol roztok správne vstreknutý a aby sa nepoškodilo kožné tkanivo.
Krok 7 - Vyberte injekčnú striekačku
Rýchlo vytiahnite injekčnú striekačku a na miesto vpichu zatlačte tampónom navlhčeným v dezinfekčnom prostriedku. Ľahká masáž časti - udržiavanie tlaku - pomôže rozptýleniu roztoku Puregon a zmierni nepohodlie. Akékoľvek zvyšky roztoku musia byť Nemiešajte Puregon s inými liekmi.
Ak zabudnete použiť Puregon
Ak ste zabudli užiť dávku, neužívajte dvojnásobnú dávku, aby ste nahradili vynechanú dávku.
Kontaktujte svojho lekára. Ak máte ďalšie otázky týkajúce sa použitia tohto lieku, opýtajte sa svojho lekára.
Predávkovanie Čo robiť, ak ste užili príliš veľa Puregonu
Ak použijete viac Puregonu, ako máte
Okamžite to povedzte svojmu lekárovi. Príliš vysoká dávka Puregonu môže spôsobiť nadmernú stimuláciu vaječníkov (OHSS). To sa môže prejaviť bolesťou žalúdka. Ak máte bolesti žalúdka, ihneď to povedzte svojmu lekárovi.
Pozri tiež časť 4 Možné vedľajšie účinky.
Vedľajšie účinky Aké sú vedľajšie účinky lieku Puregon
Tak ako všetky lieky, aj tento liek môže spôsobovať vedľajšie účinky, hoci sa neprejavia u každého.
Vážne vedľajšie účinky u žien
Komplikáciou liečby FSH je „nadmerná stimulácia vaječníkov.“ Nadmerná stimulácia vaječníkov môže mať za následok vznik zdravotného stavu nazývaného ovariálny hyperstimulačný syndróm (OHSS), ktorý môže predstavovať vážny zdravotný problém. Riziko je možné znížiť starostlivým sledovaním vývoja folikulov počas liečby. Váš lekár vykoná ultrazvukové vyšetrenie vaječníkov, aby pozorne sledoval počet dozrievajúcich folikulov. Lekár môže tiež skontrolovať hladiny hormónov v krvi. Prvými príznakmi sú bolesť žalúdka, nevoľnosť alebo hnačka. V závažnejších prípadoch môžu príznaky zahŕňať zväčšenie vaječníkov, nahromadenie tekutiny v bruchu a / alebo hrudníku (čo môže spôsobiť náhly prírastok hmotnosti v dôsledku hromadenia tekutín) a tvorbu cirkulujúcich krvných zrazenín.
Pozrite si časť Varovania a opatrenia v časti 2.
Ihneď navštívte lekára, ak máte bolesti žalúdka alebo akékoľvek iné príznaky ovariálnej hyperstimulácie, aj keď k tomu dôjde niekoľko dní po poslednej injekcii.
Ak ste žena:
Časté vedľajšie účinky (môžu postihnúť až 1 z 10 ľudí)
- Bolesť hlavy
- Reakcie v mieste vpichu (ako je pálenie, bolesť, začervenanie, opuch a svrbenie)
- Ovariálny hyperstimulačný syndróm (OHSS)
- Bolesť panvy
- Bolesť žalúdka a / alebo nadúvanie
Menej časté vedľajšie účinky (môžu postihnúť až 1 zo 100 ľudí)
- Nepohodlie v prsníkoch (vrátane citlivosti)
- Hnačka, zápcha alebo žalúdočné ťažkosti
- Zväčšenie maternice
- Necítiť sa dobre
- Reakcie z precitlivenosti (ako vyrážka, začervenanie, žihľavka a svrbenie)
- Ovariálne cysty alebo zväčšené vaječníky
- Torzia vaječníkov (skrútenie vaječníkov)
- Vaginálne krvácanie
Zriedkavé vedľajšie účinky (môžu postihnúť až 1 z 1 000 ľudí)
Krvné zrazeniny (k tomu môže dôjsť aj pri absencii nedobrovoľnej nadmernej stimulácie vaječníkov, pozri Upozornenia a opatrenia v časti 2).
Hlásilo sa aj tehotenstvo mimo maternice (mimomaternicové tehotenstvo), potrat a viacpočetné tehotenstvo. Tieto vedľajšie účinky sa nepovažujú za súvisiace s používaním Puregonu, ale s technológiou asistovanej reprodukcie (ART) alebo s následným tehotenstvom.
Ak ste muž:
Časté vedľajšie účinky (môžu postihnúť až 1 z 10 ľudí)
- Akné
- Reakcie v mieste vpichu (ako je tvrdnutie a bolesť)
- Bolesť hlavy
- Vyrážka
- Zväčšenie mliečnej žľazy
- Testikulárna cysta
Hlásenie vedľajších účinkov
Ak sa u vás vyskytne akýkoľvek vedľajší účinok, obráťte sa na svojho lekára alebo lekárnika. To sa týka aj akýchkoľvek vedľajších účinkov, ktoré nie sú uvedené v tejto písomnej informácii. Vedľajšie účinky môžete hlásiť aj priamo prostredníctvom národného systému hlásenia uvedeného v Prílohe V. Hlásením vedľajších účinkov môžete prispieť k získaniu ďalších informácií o bezpečnosti tohto lieku.
Expirácia a retencia
Tento liek uchovávajte mimo dohľadu a dosahu detí.
Skladovanie v lekárni
Uchovávajte pri 2 ° C - 8 ° C (v chladničke). Neuchovávajte v mrazničke.
Skladovanie u pacienta
Má dve možnosti:
- Uchovávajte pri 2 ° C - 8 ° C (v chladničke). Neuchovávajte v mrazničke.
- Skladujte pri teplote 25 ° C alebo nižšej (izbová teplota) počas jedného obdobia nepresahujúceho 3 mesiace.
Poznamenajte si, kedy začnete výrobok skladovať mimo chladničky.
Injekčné liekovky uchovávajte vo vonkajšom obale.
Obsah injekčnej liekovky sa má použiť ihneď po prepichnutí gumovej zátky ihlou.
Nepoužívajte Puregon po dátume exspirácie, ktorý je uvedený na štítku a škatuli po „EXP“. Dátum exspirácie sa vzťahuje na posledný deň v danom mesiaci.
Lieky sa nesmú likvidovať odpadovou vodou alebo domovým odpadom. Opýtajte sa svojho lekárnika, ako zlikvidovať lieky, ktoré už nepoužívate. Pomôže to chrániť životné prostredie.
Ďalšie informácie
Čo Puregon obsahuje
Účinnou zložkou lieku je folitropín beta.
Puregon 50 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH), v sile 50 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Puregon 75 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako folikuly stimulujúci hormón (FSH) v sile 75 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Puregon 100 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH) v sile 100 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Puregon 150 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH) v sile 150 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Puregon 200 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH) v sile 200 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Puregon 225 IU / 0,5 ml injekčný roztok: Každá injekčná liekovka obsahuje účinnú látku folitropín beta, hormón známy ako hormón stimulujúci folikuly (FSH), v sile 225 IU v 0,5 ml vodného roztoku v injekčnej liekovke.
Ďalšie zložky sú sacharóza, citrát sodný, L-metionín a polysorbát 20 vo vode na injekciu. PH môže byť upravené hydroxidom sodným a / alebo kyselinou chlorovodíkovou.
Ako vyzerá Puregon a obsah balenia
Puregon injekčný roztok (injekcia) je číra, bezfarebná kvapalina. Dodáva sa v sklenenej injekčnej liekovke. Je dostupný v baleniach po 1, 5 alebo 10 injekčných liekovkách.
Na trh nemusia byť uvedené všetky veľkosti balenia.
Zdrojový leták: AIFA (Talianska agentúra pre lieky). Obsah zverejnený v januári 2016. Súčasné informácie nemusia byť aktuálne.
Aby ste mali prístup k najaktuálnejšej verzii, odporúča sa navštíviť webovú stránku AIFA (Talianska agentúra pre lieky). Vylúčenie zodpovednosti a užitočné informácie.
01.0 NÁZOV LIEKU
PUREGON 50 IU / 0,5 ml ROZTOK NA INJEKCIU
02.0 KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Jedna injekčná liekovka obsahuje 50 IU rekombinantného hormónu stimulujúceho folikuly (FSH) v 0,5 ml vodného roztoku. To zodpovedá dávke 100 IU / ml. Jedna injekčná liekovka obsahuje 5 mcg bielkovín (špecifická bioaktivita in vivo čo zodpovedá približne 10 000 IU FSH / mg bielkovín). Injekčný roztok obsahuje účinnú látku folitropín beta, ktorá je vyrobená genetickým inžinierstvom z bunkovej línie vaječníkov čínskeho škrečka (CHO).
Úplný zoznam pomocných látok, pozri časť 6.1.
03.0 LIEKOVÁ FORMA
Injekčný roztok (prípravok na injekciu).
Číry a bezfarebný roztok.
04.0 KLINICKÉ INFORMÁCIE
04.1 Terapeutické indikácie
V žene:
Puregon je indikovaný na liečbu ženskej neplodnosti v nasledujúcich klinických stavoch:
Anovulácia (vrátane syndrómu polycystických ovárií, PCOS) u žien, ktoré nereagovali na liečbu citrátom klomifénu.
Riadená hyperstimulácia vaječníkov na vyvolanie vývoja viacerých folikulov v protokoloch asistovanej reprodukcie [napr. hnojenie in vitro/ prenos embrya (IVF / ET), intratubálny prenos gamét (GIFT) a intracytoplazmatická injekcia spermií (ICSI)].
V „človeku:
Nedostatočná spermatogenéza v dôsledku hypogonadotropného hypogonadizmu.
04.2 Dávkovanie a spôsob podávania
Liečba Puregonom sa má začať pod dohľadom lekára so skúsenosťami s liečbou problémov s plodnosťou.
Prvá injekcia Puregonu sa musí podať pod priamym lekárskym dohľadom.
Dávkovanie
Dávkovanie u žien
V odpovedi vaječníkov na exogénne gonadotropíny existujú u toho istého jedinca a medzi rôznymi jedincami značné rozdiely. To znemožňuje definovať jeden rozvrh dávkovania. Dávky je preto potrebné individuálne upraviť podľa odpovede vaječníkov. To si vyžaduje ultrazvukové vyšetrenie a monitorovanie hladín estradiolu.
Na základe výsledkov komparatívnych klinických štúdií sa odporúča podávať nižšiu celkovú dávku Puregonu na kratšiu dobu liečby, než sa obvykle používa pre močový FSH, a to nielen na optimalizáciu vývoja folikulov, ale aj na zníženie, aby sa minimalizovalo riziko nechcená ovariálna hyperstimulácia (pozri časť 5.1).
Klinická skúsenosť s Puregonom je založená na období až troch terapeutických cyklov pre obe indikácie. Kombinovaná skúsenosť s IVF naznačuje, že stupeň úspešnosti liečby spravidla zostáva počas prvých štyroch pokusov nezmenený, potom sa postupne znižuje.
Anovulácia
Vo všeobecnosti sa odporúča sekvenčný liečebný režim, ktorý začína denným podávaním 50 IU Puregonu najmenej 7 dní. Ak nedôjde k ovariálnej odpovedi, denná dávka sa postupne zvyšuje, až kým rast folikulov a / alebo plazmatické hladiny estradiolu nenaznačia „adekvátnu farmakodynamickú odpoveď. Denné zvýšenie hladín estradiolu o 40-100% sa považuje za optimálne.
Denná dávka sa podáva, kým sa nedosiahnu predovulačné podmienky, t. J. Pokiaľ nie je na ultrazvuku dôkaz o dominantnom folikulu s priemerom najmenej 18 mm a / alebo keď sa plazmatické hladiny estradiolu zvýšia na 300-900. Pikogramov / ml (1 000- 3000 pmol / l). Na dosiahnutie tohto stavu zvyčajne postačuje 7-14 dní liečby. Podávanie Puregonu sa potom zastaví a ovuláciu je možné vyvolať podaním ľudského chorionického gonadotropínu (hCG).
Ak je počet vyzretých folikulov príliš vysoký alebo hladiny estradiolu stúpajú príliš rýchlo, t. J. Viac ako dvojnásobne každý deň, počas 2 alebo 3 po sebe nasledujúcich dní estradiolu, dennú dávku je potrebné znížiť.
Pretože folikuly s priemerom väčším ako 14 mm môžu viesť k tehotenstvu, viac predovulačných folikulov väčších ako 14 mm predstavuje riziko viacpočetného tehotenstva. V tomto prípade by sa hCG nemalo podávať a malo by sa zabrániť počatiu, aby sa zabránilo viacnásobnému tehotenstvu.
Riadená ovariálna hyperstimulácia v programoch asistovanej reprodukcie.
Existuje množstvo stimulačných protokolov. Odporúča sa počiatočná dávka 100-225 IU, najmenej počas prvých 4 dní. Dávku je potom možné individuálne upraviť na základe reakcie vaječníkov. V klinických štúdiách sa zistilo, že udržiavacie dávky v rozmedzí od 75 do 375 IU počas 6 až 12 dní sú dostatočné, aj keď môže byť potrebná dlhšia liečba.
Puregon sa môže podávať samotný alebo, aby sa zabránilo včasnej luteinizácii, v kombinácii s agonistom alebo antagonistom GnRH. Pri použití agonistu GnRH môže byť potrebná vyššia celková dávka Puregonu na dosiahnutie „adekvátnej folikulárnej odpovede“.
Ovariálna odpoveď sa monitoruje ultrazvukom a stanovením hladín estradiolu v plazme. Keď ultrazvukové vyhodnotenie indikuje prítomnosť najmenej 3 folikulov s priemerom 16 až 20 mm a existujú dôkazy o dobrej odpovedi estradiolu (plazmatické hladiny približne 300-400 pikogramov / ml (1 000-1 300 pmol / l) pre každý folikul s s priemerom väčším ako 18 mm), konečná fáza dozrievania folikulov sa vyvolá podaním hCG. Získanie vajíčka sa vykoná o 34 až 35 hodín neskôr.
Dávkovanie u človeka
Puregon sa má podávať v dávke 450 IU / týždeň, najlepšie rozdelených do 3 dávok po 150 IU, súbežne s podávaním hCG. Liečba Puregonom a hCG by mala pokračovať najmenej 3 až 4 mesiace, než bude možné pozorovať zlepšenie spermatogenézy. Na vyhodnotenie odpovede sa odporúča analýza spermy 4 až 6 mesiacov po začiatku liečby. Ak pacient do tejto doby neodpovie, môže sa v kombinovanej terapii pokračovať; Súčasné klinické skúsenosti naznačujú, že na dosiahnutie spermatogenézy môže byť potrebná liečba až 18 mesiacov alebo viac.
Neexistujú žiadne údaje o použití Puregonu u detí.
Spôsob podávania
Aby sa zabránilo bolestivému podaniu injekcie a aby sa minimalizovalo riziko úniku tekutiny z miesta vpichu, Puregon sa má podávať pomaly intramuskulárne alebo subkutánne. Aby sa zabránilo lipoatrofii, má sa podať subkutánna injekcia na iné miesto. Všetky zvyšky roztoku sa majú zlikvidovať.
Subkutánnu injekciu Puregonu si môže podať pacient sám alebo iná osoba po adekvátnom poučení lekára. Samoriadenie Puregonu môžu vykonávať len dobre motivovaní pacienti, adekvátne vyškolení a s možnosťou získať odbornú radu.
04.3 Kontraindikácie
Pre mužov a ženy
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
Nádory vaječníkov, prsníkov, maternice, semenníkov, hypofýzy alebo hypotalamu.
Primárna nedostatočnosť pohlavných žliaz.
Tiež pre ženu
Vaginálne krvácanie, ktoré nebolo diagnostikované.
Ovariálne cysty alebo zväčšenie vaječníkov nie je spôsobené syndrómom polycystických vaječníkov (PCOS).
Malformácie reprodukčných orgánov nezlučiteľné s tehotenstvom.
Fibroidné nádory maternice nekompatibilné s tehotenstvom.
04.4 Špeciálne upozornenia a vhodné opatrenia pri používaní
Puregon môže obsahovať stopy streptomycínu a / alebo neomycínu. Tieto antibiotiká môžu u citlivých osôb spôsobiť reakcie z precitlivenosti.
Je potrebné vylúčiť prítomnosť nekontrolovaných extragonadálnych endokrinopatií (napr. Dysfunkcia štítnej žľazy, nadobličiek alebo hypofýzy).
V žene
U gravidít získaných po indukcii ovulácie gonadotropnými prípravkami existuje zvýšené riziko viacpočetných tehotenstiev. Primeraná úprava dávky FSH by mala zabrániť vzniku viacpočetných folikulov. Viacnásobné tehotenstvá, najmä tie s veľkým počtom plodov, vedú k zvýšenému riziku nežiaducich účinkov. materské a perinatálne výsledky Pred začatím liečby majú byť pacienti poučení o možných rizikách viacnásobného pôrodu.
Pretože neplodné ženy podstupujúce asistované oplodnenie, najmä IVF, majú často tubulárne abnormality, výskyt mimomaternicových tehotenstiev môže byť vyšší. Preto je dôležité včasným ultrazvukom potvrdiť, že ide o vnútromaternicové tehotenstvo.
Miera straty tehotenstva u žien podstupujúcich techniky asistovanej reprodukcie je vyššia ako v normálnej populácii.
Incidencia vrodených malformácií po technikách asistovanej reprodukcie môže byť o niečo vyššia ako incidencia pozorovaná po spontánnom počatí, čo môže byť spôsobené rozdielmi v rodičovských charakteristikách (napr. Vek matky, charakteristiky spermií) a viacpočetnými gestáciami.
Nežiaduca ovariálna hyperstimulácia: Pri liečbe žien sa má pred liečbou a v pravidelných intervaloch počas liečby vykonávať ultrazvukové vyhodnotenie vývoja folikulov a stanovenie hladín estradiolu. Bez ohľadu na vývoj veľkého počtu folikulov sa hladiny estradiolu môžu extrémne rýchlo zvyšovať, napríklad viac ako dvojnásobne každý deň počas 2 alebo 3 po sebe nasledujúcich dní a nakoniec dosiahnuť nadmerne vysoké hodnoty. Diagnózu hyperstimulácie vaječníkov je možné potvrdiť ultrazvukom. Ak dôjde k nežiaducej ovariálnej hyperstimulácii (t.j. nie ako súčasť programu asistovanej reprodukcie), podávanie Puregonu sa má prerušiť. V tomto prípade sa treba vyhnúť počatiu a hCG by sa nemalo podávať, pretože môže okrem viacnásobnej ovulácie vyvolať aj ovariálny hyperstimulačný syndróm (OHSS). Klinickými príznakmi a znakmi mierneho ovariálneho hyperstimulačného syndrómu sú bolesť brucha, nevoľnosť, hnačka a mierne alebo stredne závažné zväčšenie vaječníkov s prítomnosťou cystických útvarov. V súvislosti so syndrómom ovariálnej hyperstimulácie boli hlásené prechodné odchýlky v testoch funkcie pečene, ktoré naznačujú dysfunkciu pečene a môžu byť sprevádzané morfologickými zmenami v biopsii pečene. V zriedkavých prípadoch môže závažný ovariálny hyperstimulačný syndróm ohroziť život. V týchto prípadoch je charakteristická prítomnosť veľkých ovariálnych cýst (majú tendenciu prasknúť), ascitu, často hydrotoraxu a prírastku hmotnosti. V zriedkavých prípadoch sa v súvislosti s OHSS môže vyskytnúť venózny alebo arteriálny tromboembolizmus.
Po liečbe folitropínom beta a po liečbe inými gonadotropínmi bolo hlásené skrútenie vaječníkov. To môže byť spojené s ďalšími rizikovými faktormi, ako je OHSS, tehotenstvo, predchádzajúca operácia brucha, anamnéza torzie vaječníkov, predchádzajúca alebo súčasná ovariálna cysta a vaječníky. Polycystický vaječník poškodenie spôsobené zníženým prísunom krvi môže byť obmedzené včasnou diagnostikou a okamžitou detoráciou.
Existujú správy o benígnych aj malígnych novotvaroch na vaječníkoch a iných reprodukčných systémoch u žien, ktoré podstúpili viacero liečebných terapií na liečbu neplodnosti. Zatiaľ nebolo stanovené, či liečba gonadotropínmi zvyšuje základné riziko týchto rakovín u neplodných žien alebo nie.
Ženy so všeobecne uznávanými rizikovými faktormi trombózy, ako sú osobná alebo rodinná anamnéza, závažná obezita (index telesnej hmotnosti> 30 kg / m2) alebo známa trombofília, môžu mať zvýšené riziko venóznych alebo arteriálnych tromboembolických príhod počas alebo po liečbe gonadotropínmi. U týchto žien je potrebné zvážiť prínos liečby IVF voči rizikám, treba však pamätať na to, že samotné tehotenstvo môže viesť k zvýšenému riziku trombózy.
V „človeku
U mužov svedčí zvýšená hladina endogénneho FSH o primárnom testikulárnom zlyhaní. Títo pacienti nereagujú na liečbu Puregon / hCG.
04.5 Interakcie s inými liekmi a iné formy interakcie
Súbežné používanie Puregonu a klomiféncitrátu môže zvýšiť folikulárnu odpoveď.
Po supresii hypofýzy vyvolanej agonistom GnRH môže byť potrebná vyššia dávka Puregonu na dosiahnutie adekvátnej folikulárnej odpovede.
04.6 Gravidita a laktácia
Plodnosť
Puregon sa používa na liečbu žien podstupujúcich ovariálnu indukciu alebo kontrolovanú ovariálnu hyperstimuláciu v programoch asistovanej reprodukcie. U mužov sa Puregon používa na liečbu nedostatočnej spermatogenézy spôsobenej hypogonadotropným hypogonadizmom. Dávkovanie a spôsob podávania, pozri časť 4.2.
Tehotenstvo
Neexistujú žiadne indikácie na použitie Puregonu počas gravidity. V klinickom použití po ovariálnej hyperstimulácii ovanizovanej gonadotropínmi nebolo hlásené žiadne teratogénne riziko. V prípade expozície počas gravidity nie sú klinické údaje dostatočné na vylúčenie teratogénneho účinku rekombinantného FSH. Doteraz však nebol hlásený žiadny osobitný malformačný účinok. V štúdiách na zvieratách sa nepozoroval žiadny teratogénny účinok.
Čas kŕmenia
Z klinických štúdií a štúdií na zvieratách nie sú dostupné informácie o vylučovaní folitropínu beta do materského mlieka. Follitropín beta nie je pravdepodobné, že sa vylučuje do ľudského mlieka kvôli jeho vysokej molekulovej hmotnosti. Ak by sa follitropín beta vylučoval do ľudského mlieka, degradoval by sa v črevnom trakte dieťaťa. Follitropín beta môže ovplyvniť produkciu mlieka.
04.7 Účinky na schopnosť viesť vozidlá a obsluhovať stroje
Puregon nemá žiadny alebo má zanedbateľný vplyv na schopnosť viesť vozidlá alebo obsluhovať stroje.
04.8 Nežiaduce účinky
Klinické použitie Puregonu intramuskulárne alebo subkutánne môže spôsobiť lokálne reakcie v mieste vpichu injekcie (3% všetkých liečených pacientov). Väčšina týchto lokálnych reakcií je stredne závažná a má prechodný charakter. Boli pozorované generalizované reakcie z precitlivenosti. Zriedkavejšie (približne 0,2% všetci pacienti liečení Puregonom).
Liečba ženy: Známky a symptómy súvisiace so syndrómom ovariálnej hypestimulácie boli hlásené u približne 4% žien liečených Puregonom v klinických skúšaniach (pozri časť 4.4). Vedľajšie účinky súvisiace s týmto syndrómom zahŕňajú panvovú bolesť a / alebo kongesciu, bolesť brucha a / alebo distenziu, nepríjemné pocity v prsníkoch a zväčšenie vaječníkov.
Nasledujúca tabuľka uvádza nežiaduce reakcie Puregonu hlásené v klinických štúdiách u žien podľa triedy orgánových systémov a frekvencie; časté (≥ 1/100,
1 Poruchy prsníka zahŕňajú citlivosť, bolesť a / alebo kongesciu a bolesť bradaviek
2 Lokálne reakcie v mieste vpichu zahŕňajú: pálenie, bolesť, začervenanie, opuch a svrbenie
3 K generalizovaným reakciám z precitlivenosti patria: erytém, žihľavka, vyrážka a svrbenie.
Tiež bolo hlásené mimomaternicové tehotenstvo, potrat a viacpočetné tehotenstvo. Tieto sa považujú za súvisiace s postupom ART alebo následným tehotenstvom.
V zriedkavých prípadoch je tromboembolizmus spojený s liečbou Puregon / hCG. Toto bolo tiež hlásené počas liečby inými gonadotropínmi.
Liečba človeka: Nasledujúca tabuľka uvádza nežiaduce reakcie Puregonu hlásené v klinických skúšaniach u mužov (30 liečených pacientov) podľa triedy orgánových systémov a frekvencie; časté (≥ 1/100,
1. Nežiaduce reakcie, ktoré sú hlásené iba raz, sú uvedené ako časté, pretože jedna správa zvyšuje frekvenciu nad 1%.
2. Lokálne reakcie v mieste vpichu zahŕňajú stvrdnutie a bolesť.
04,9 Predávkovanie
Neexistujú žiadne údaje o akútnej toxicite Puregonu u ľudí; V štúdiách na zvieratách sa však ukázalo, že akútna toxicita Puregonu a močových gonadotropínových prípravkov je veľmi nízka. Príliš vysoká dávka FSH môže viesť k hyperstimulácii vaječníkov (pozri časť 4.4).
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: pohlavné hormóny a modulátory genitálneho systému, gonadotropíny, ATC kód: G03G A06.
Puregon obsahuje rekombinantný FSH. Je produkovaná bunkovou líniou vaječníkov čínskeho škrečka modifikovanou podjednotkami ľudského génu FSH pomocou techniky rekombinantnej DNA. Sekvencia primárnych aminokyselín je rovnaká ako v prírodnom ľudskom FSH. Je známe, že v uhľohydrátovom reťazci sú malé rozdiely.
FSH je zásadný pre normálny rast a dozrievanie folikulov a pre gonadálnu steroidogenézu. U žien je množstvo FSH rozhodujúce pre začatie a trvanie vývoja folikulov a následne pre počet a časovú koordináciu folikulov, ktoré dosiahnu dospelosť. Puregon sa preto môže vo vybraných prípadoch zhoršenej funkcie gonád použiť na stimuláciu vývoja folikulov a na podporu produkcie steroidov.
Puregon sa navyše môže použiť na indukciu vývoja viacerých folikulov v programoch asistovanej reprodukcie, ako je napríklad hnojenie in vitro/ prenos embrya (IVF / ET), intratubálny prenos gamét (GIFT) a intracytoplazmatická injekcia spermií (ICSI).
Po liečbe Puregonom spravidla nasleduje podanie hCG na indukciu konečnej fázy dozrievania folikulov, obnovenia meiózy a prasknutia folikulu.
V klinických štúdiách porovnávajúcich rekombinantný FSH (folitropín beta) a močový FSH na kontrolovanú stimuláciu vaječníkov u žien zúčastňujúcich sa na protokoloch asistovanej reprodukcie (ART) a na indukciu ovulácie (pozri tabuľky 1 a 2 nižšie) bol Puregon účinnejší ako močový FSH, pokiaľ ide o nižšiu celkovú dávku a kratšiu dobu liečby potrebnú na spôsobenie dozrievania folikulov.
Pokiaľ ide o kontrolovanú ovariálnu stimuláciu, Puregon viedol k vyššiemu počtu oocytov odobratých pri nižšej celkovej dávke a s kratším obdobím liečby v porovnaní s močovým FSH.
Tabuľka 1: Výsledky štúdie 37608 (randomizovaná, porovnávacia štúdia porovnávajúca bezpečnosť a účinnosť Puregonu s močovým FSH pri kontrolovanej ovariálnej stimulácii).
* Rozdiely medzi týmito 2 skupinami boli štatisticky významné (s
Pokiaľ ide o indukciu ovulácie, Puregon mal za následok nižšiu priemernú celkovú dávku a kratšiu priemernú dĺžku liečby ako FSH v moči.
Tabuľka 2: Výsledky štúdie 37609 (randomizovaná, porovnávacia štúdia porovnávajúca bezpečnosť a účinnosť Puregonu s močovým FSH pri indukcii ovulácie).
* Rozdiely medzi týmito 2 skupinami boli štatisticky významné (s
a Obmedzené na ženy s indukovanou ovuláciou (Puregon, n = 76; močový FSH, n = 42).
05.2 Farmakokinetické vlastnosti
Po intramuskulárnom alebo subkutánnom podaní Puregonu sa maximálne koncentrácie FSH dosiahnu približne do 12 hodín. Po intramuskulárnom podaní Puregonu sú maximálne koncentrácie FSH vyššie a dosahujú sa skôr u mužov ako u žien. Vzhľadom na predĺžené uvoľňovanie z miesta vpichu a polčas eliminácie približne 40 hodín (12-70 hodín) zostávajú hladiny FSH zvýšené počas 24-48 hodín. Vzhľadom na relatívne vysoký polčas eliminácie po opakovanom podávaní rovnaké dávky, plazmatické koncentrácie FSH sú približne 1,5-2,5 krát vyššie ako tie, ktoré sa vyskytujú po jednom podaní. Toto zvýšenie prispieva k dosiahnutiu terapeutických hladín FSH.
Medzi intramuskulárnym a subkutánnym podaním Puregonu nie sú žiadne významné farmakokinetické rozdiely. Oba majú absolútnu biologickú dostupnosť približne 77%. Pretože rekombinantný FSH je veľmi biochemicky podobný ľudskému FSH, je distribuovaný, metabolizovaný a vylučovaný rovnakým spôsobom.
05.3 Predklinické údaje o bezpečnosti
Jednorazové podanie Puregonu u potkanov nevyvolalo významné toxické účinky. V štúdiách opakovaného podávania potkanom (2 týždne) a psom (13 týždňov) v dávkach až 100 -násobku maximálnej dávky pre ľudí nespôsobil Puregon významné toxické účinky.
Puregon nepreukázal mutagénnu silu ani v Amesovom teste, ani v teste chromozomálnej aberácie s ľudskými lymfocytmi. in vitro.
06.0 FARMACEUTICKÉ INFORMÁCIE
06.1 Pomocné látky
Injekčný roztok Puregon obsahuje:
sacharóza
citrát sodný
L-metionín
polysorbát 20
voda na injekciu.
Na úpravu pH sa môže pridať hydroxid sodný a / alebo kyselina chlorovodíková.
06.2 Nekompatibilita
Pretože neexistujú štúdie inkompatibility, liek sa nesmie miešať s inými výrobkami.
06.3 Obdobie platnosti
3 roky.
Obsah injekčnej liekovky sa má použiť ihneď po prepichnutí gumovej zátky ihlou.
06.4 Špeciálne opatrenia na uchovávanie
Uchovávajte v chladničke (2 ° C - 8 ° C).
Neuchovávajte v mrazničke.
Injekčné liekovky uchovávajte vo vonkajšom obale.
Pre pohodlie pacienta môže Puregon pacient uchovávať sám pri teplotách nepresahujúcich 25 ° C počas jedného obdobia nepresahujúceho 3 mesiace.
06.5 Charakter vnútorného obalu a obsahu balenia
0,5 ml roztoku v 3 ml injekčnej liekovke (sklo typu I) so zátkou (chlórbutylová guma).
Balenie 1, 5 alebo 10.
Na trh nemusia byť uvedené všetky veľkosti balenia.
06.6 Návod na použitie a zaobchádzanie
Roztok nepoužívajte, ak sú v ňom častice alebo ak nie je číry.
Obsah injekčnej liekovky sa má použiť ihneď po prepichnutí gumovej zátky ihlou.
Nepoužitý liek a odpad z tohto lieku musí byť zlikvidovaný v súlade s miestnymi predpismi.
07.0 DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
N.V. Organon, Kloosterstraat 6, Postbus 20, 5340 BH Oss, Holandsko
08.0 REGISTRAČNÉ ČÍSLO
EU/1/96/008/17
029520172
EU/1/96/008/18
029520184
EU/1/96/008/19
029520196
09.0 DÁTUM PRVEJ REGISTRÁCIE ALEBO OBNOVENIA REGISTRÁCIE
Dátum prvej registrácie: 3. mája 1996
Dátum posledného obnovenia: 3. mája 2006
10.0 DÁTUM REVÍZIE TEXTU
11/2010